* 前言:
有这么一项技术,一经推出即被称为美国“硅谷圣经”的科技企业杂志《Red Herring》评选为“2018 Top North America”榜单;同年,生物医药领域的权威杂志《The Scientist》将 其评选为当年的十大创新技术。
此外,顶级癌症研究结构,包括M.D.安德森癌症中心、纪念斯隆-凯特琳癌症中心、美国癌症研究中心等纷纷为其背书。短短几年,此技术足迹已经遍布全球30个国家。2019年7月来到中国,携手诺禾致源达成深度战略合作。
这个传奇的技术便是单细胞 DNA 分析平台 TapestriTM,于2017年被位于美国加州的Mission Bio推出。该平台基于微流控原理,可检测到癌症中1%的稀有细胞以及在癌症治疗期间突变的共同发生, 为个体化提供实际指导。
借着Mission Bio 首席商务官Darrin Crisitell应邀来China Focus@San Francisco 路演专场分享其成功商业模式以及创新技术的契机,美柏医健针对单细胞测序行业进行全面剖析,带您走近这个神秘的 “高大上” 新兴领域。



识别二维码,了解路演专场



识别二维码,进入会议报名
本文有13000字,阅读时间大概需要20分钟!
* 目录:
1. 背景介绍
2. 市场分析
3. 应用领域
4. 核心技术原件
5. 产业链核心玩家的技术PK
6. 瓶颈及挑战
1.背景介绍
传统的测序(DNA测序、RNA测序、蛋白测序、表观基因、代谢组、微生物组)是基于细胞群体,提供的信息是成千上万细胞的一个稳态的平均值。这种测序方法忽视了细胞的异质性(每个细胞的单一独特性),以及小群体细胞的重要功能性。在人体的每一个组织中,都拥有着大量不同的细胞类型,每一种细胞类型有着独特的起源和功能,而它的谱系和发展的状态又决定了每个细胞如何和周围的微环境如何相互作用。
于是单细胞测序技术(Single Cell Sequencing, SCS)应运而生,有望解决人类生物学和医学中尚未解决的核心问题,那就是关于人类细胞在发育,生长,更新,衰老和疾病中的结构,动力学和变异性。
单细胞测序是一项相对较新的技术。一直到 2009年,才发表了首个单细胞RNA测序(RNA-seq)数据。2013年,自然杂志授予单细胞测序年度技术荣誉,认为该技术将改变和引领生物界和医学界的众多领域。
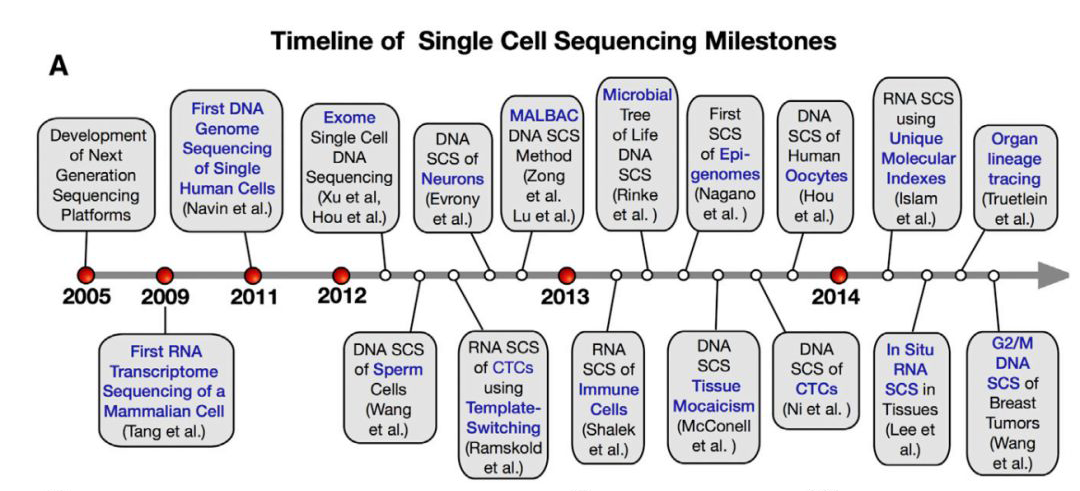


▲Mol Cell. 2015 May 21;58(4):598-609
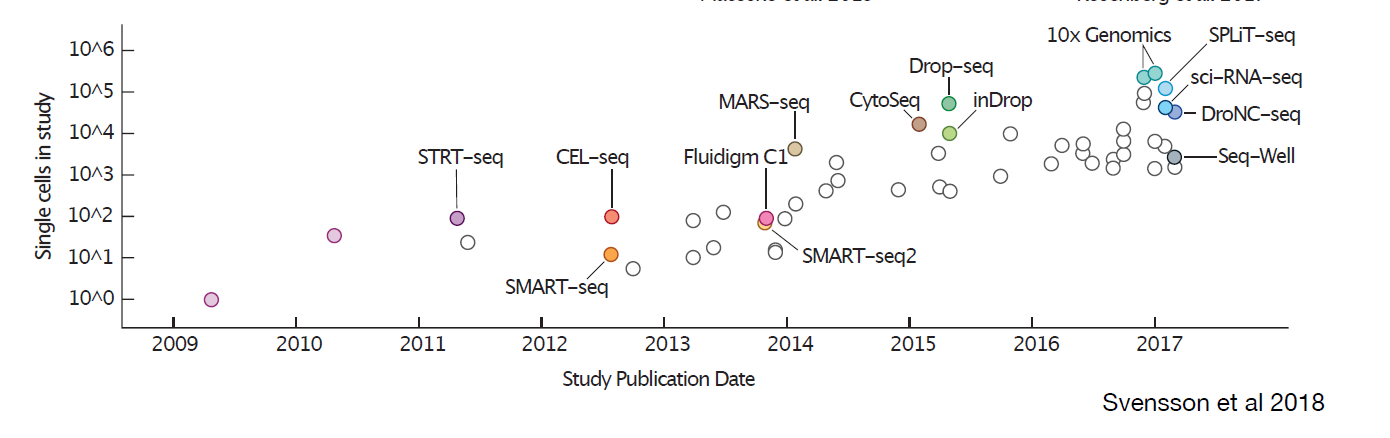


2.市场分析
2018年单细胞测序的市场价值为18.3亿美元,复合年均增长率 (CAGR) 约为16.5%,预计到2025年将达到53. 2亿美元。北美在2019年占全球市场价值的约45.4%,欧洲地区占26.52%。北美的优势主要归因于该地区创新生物技术和生物制药公司的建立能促进区域市场的增长。亚太地区预计将在预测期内实现最快的增长,这归功于政府为改善医疗基础设施而采取的众多举措,熟练的专业人员操作先进的分析仪器的能力以及医疗支出的增加。
关于单细胞分析的文章发表在过去的几年也有着爆发性的增长。目前,约有1300项临床试验正在进行中,主要是评估单细胞测序在诊断各种类型的癌症和感染(包括HIV,肝炎和流感)中的功效,以及在干细胞移植手术中提高成功率的应用。
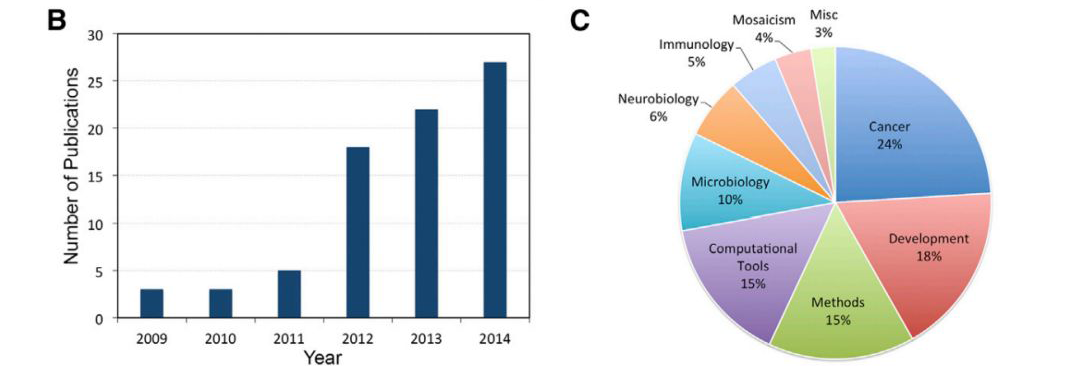


▲Mol Cell. 2015 May 21;58(4):598-609
市场的驱动主要来自几个方面:
第一,除了基因组以外,引入转录组学、蛋白质组学、代谢组学等高级设备,正在扩大单细胞测序的应用范畴。
第二,伴随着老年化趋势,例如神经类疾病,肿瘤等疾病成为了关键的社会健康问题,而在当下并无理想的治疗方案的情景下,早期诊断成为资本以及政府大力支持的领域,比如日本的Health Japan 21 以及德国的Preventive Health Care Act 法案都将极大的推动市场增长。
第三,近些年来, 精准医疗成为了未来市场的一个火拼领域。精准医疗旨在为患者量身设计出最佳治疗方案,以期达到治疗效果最大化和副作用最小化的定制医疗模式,而单细胞测序便是实现精准医疗的重要工具。 奥巴马2016年在提出了精准医疗计划。在中国,习近平总书记批示科技部和国家卫生计生委,要求国家成立中国精准医疗战略专家组。2015年科技部召开国家首次精准医学战略专家会议,会议敲定,在2030年前,中国精准医疗将投入600亿元,其中中央财政支付200亿元,企业和地方财政配套400亿元。
第四,和单细胞测序相关的技术设备的高成本在一定程度上限制了早期市场的扩展,特别是发展中及低收入国家的市场增长。随着市场、资本、创新力之间的相互成全,高端器械的成本在未来有望得到有效控制,这将成为市场增长的一个关键因素。从历史的角度来看,2003年,第一个完整的人类基因组测序成本约为27亿美元,而到如今,已经降至低于1,000美元。由此可见,基因测序的发展彻底打破了摩尔定律。
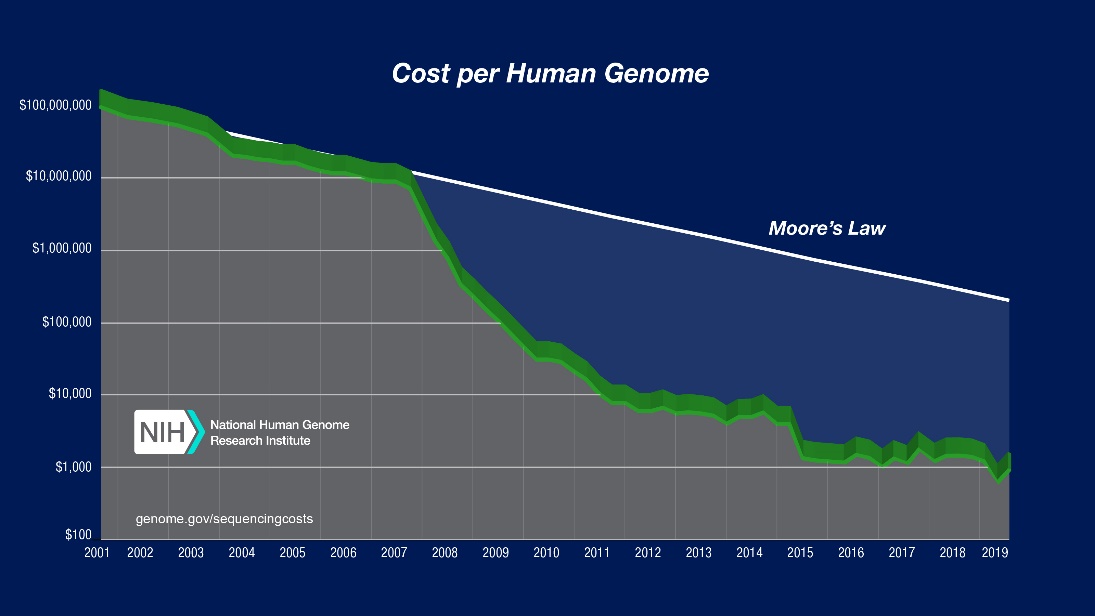


目前所有的刺激因素(政府的支持,市场的急切需求,高度的科研兴趣,生物医药巨头公司的关注等)正在解锁这个市场,单细胞基因测序行业正面临引爆点。
3.应用领域
目标人群主要包括科研机构、医院、诊断机构、以及生物技术公司和药企等。
从临床应用的角度来看,分为以下几类:
A. 肿瘤亚细胞群测序:肿瘤发生、发展过程中,细胞不断发生新的突变,形成许多亚细胞群,单细胞测序可以对这些亚细胞群进行分别的测序,并找到对应的治疗方案。其中,循环肿瘤细胞(circulating tumor cell, CTC)无创性分子诊断无疑是最有有潜力的方向。在1毫升血液中只有几个 CTC细胞,所以想通过常规的测序方法是无法实现的。迄今为止,已有研究表明,可以用单细胞RNA测序技术来判断CTC细胞是黑色素瘤细胞还是前列腺癌细胞。这些分析能让肿瘤科医生相应地改变治疗方案,而具有干细胞样表达特征的循环肿瘤细胞的靶向清除可以防止继发部位的定植和转移的形成。除此之外,有些太小而无法使用批量测序方法进行分析的小肿瘤,也可以有效的通过单细胞测序来实现。
B. 免疫细胞测序:免疫细胞在对抗原发生识别后,免疫细胞的基因组发生重排,并产生对抗原特异的抗体。对免疫细胞的测序,可以找出特异的基因结构,并发现新的免疫细胞群体,以及不同免疫细胞之间的相互作用,从而理解负责的免疫机制,为治疗提供理论基础。
C. 体外受精的胚胎测序及无创产前检测:在把胚胎植回母体之前,先取一个细胞进行测序,确认基因正常后再植回,以保证胚胎是正常的。基于MALBAC扩增技术的单细胞测序已被应用于第三代试管婴儿,成为单细胞测序技术建立最早,发展最快的临床应用。产前检测的话,可以对胎儿的核红细胞和滋养层细胞进行测序。
D. 神经类疾病的应用:在所有的疾病领域里,跟神经相关的疾病,包括老年痴呆,抑郁等一直都是最难攻克的,这和对发病机理的不确定性有很大的关系。而单分子测序提供了一种新颖的方法来对神经元细胞类型进行分类并在神经元群体中鉴定出意想不到的DNA多样性,以及其和疾病发展之间的关系。
F. 临床微生物检测:利用从患者体内获取的微生物群,利用单细胞测序技术,一方面可以对无法在实验室培养的菌群进行深度测序,另一方面也可以直接进行感染的早期诊断和耐药检测。2017年,来自美国UCSF的研究组首次实现原核生物的微生物单细胞测序技术。
G. 精准医疗:越来越多的研究表明,复杂疾病,比如肿瘤的彻底治疗一定是往精准医疗的趋势发展的。个体差异不但要求不同的治疗方法,个体差异导致的耐药性也意味着每一个特定的病人,在病情发展的不同阶段,会有独特的疾病进化模型,以及相对应的治疗方案。而这些都需要有单细胞测序的介入才能实现。
4. 单细胞测序的核心技术原件
单细胞测序技术的流程主要包括单细胞分离、细胞溶解与样品准备、基因扩增、测序与数据分析等4个方面。
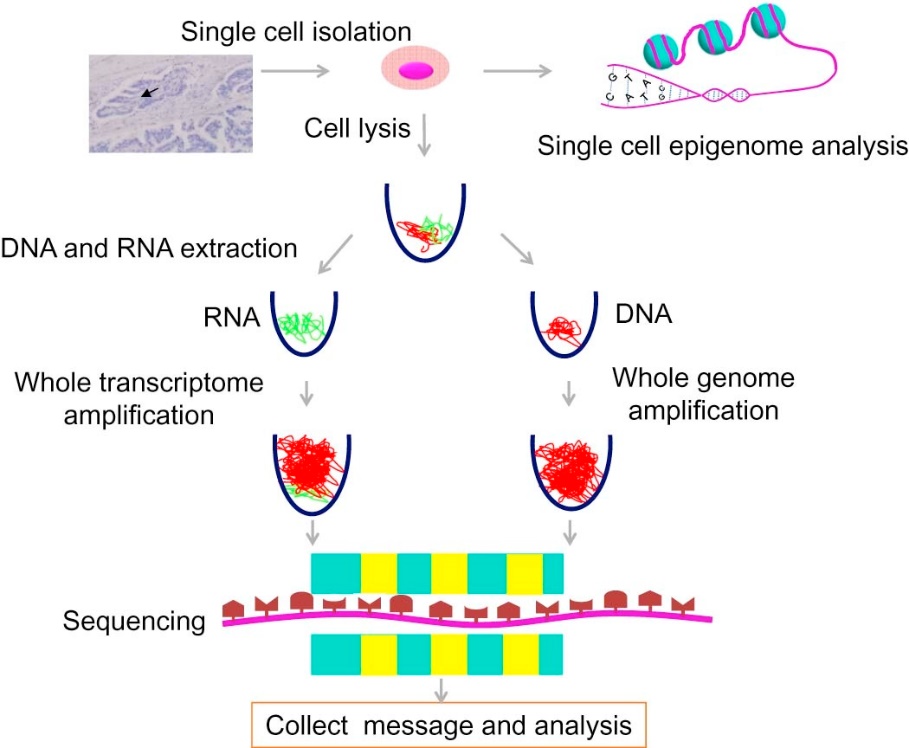


▲Cancer Lett. 2015 Aug 28;365(1):1-10.
单细胞测序分析基本流程与传统序列分析相似,目前比较高效的是基于标签(barcode)的单细胞识别,给每个细胞加上独一无二的DNA序列,这样在测序的时候,就把携带相同barcode的序列视为来自同一个细胞了,可以通过一次建库,测得数百上千个单细胞的信息。
测序与数据分析的技术不是制约单细胞测序发展的主要原因,在几代测序技术的支持下,单细胞测序在本环节的费用、速度、通量、准确度等都与其他基因测序技术差别不大。
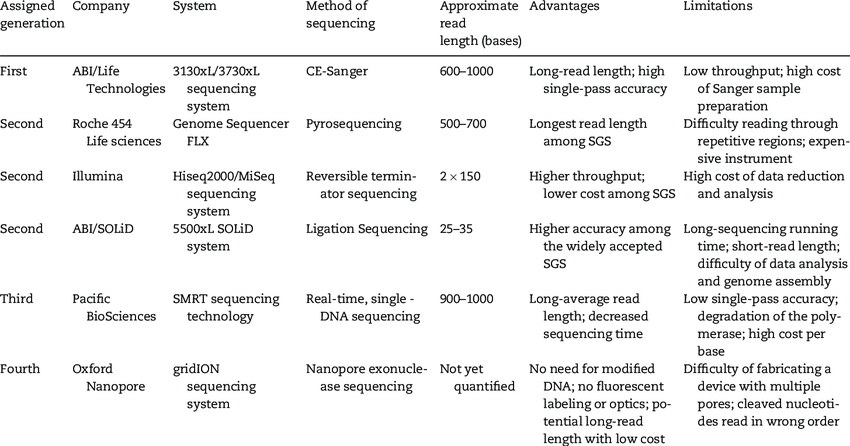


▲Brief Funct Genomics. 2019 Mar; 18(2): 119–128.
真正制约单细胞测序发展的是单细胞的检测分离与全基因组及转录组的扩增产物的质量。先说扩增,由于在单细胞中的DNA和RNA的数量非常小(几个pg),必须首先对这些分子进行扩增,同时尽量的减少错误。目前的全基因组扩增技术主要有三种:简并寡核苷酸引物PCR扩增(DOP-PCR),多重置换扩增(MDA);和基于多次退火和成环的扩增循环(MALBAC)。
用于单细胞研究的扩增技术一直存在两个问题:扩增后的偏向性和覆盖不均,部分DNA片段没有有效扩增形成可用的文库。哈佛大学谢晓亮教授团队发明结合了前两种扩增方法,通过采用包含27个核苷酸的共同序列和8个高度可变的核苷酸作为特殊引物,可以使得扩增后的DNA序列的收尾引物互补而“成环”,从而不会再次被作为模板来进行后续的PCR扩增,实现了高质量且大幅度的扩增。
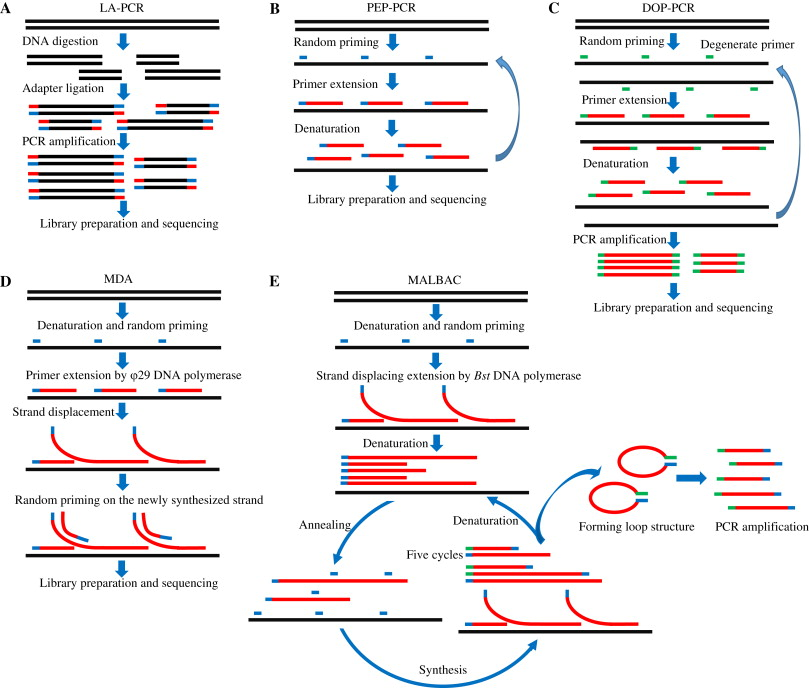


▲Genome Biol. 2018; 19: 211.
再来谈谈第二个制约的技术: 单细胞分离技术。单细胞识别和分离的技术需要满足几个要求:分离技术对细胞伤害小、分离时精确度和识别率高、操作易学、时间和成本合理等。本节将具体介绍10种现有的单细胞分离技术以及它们的优缺点。
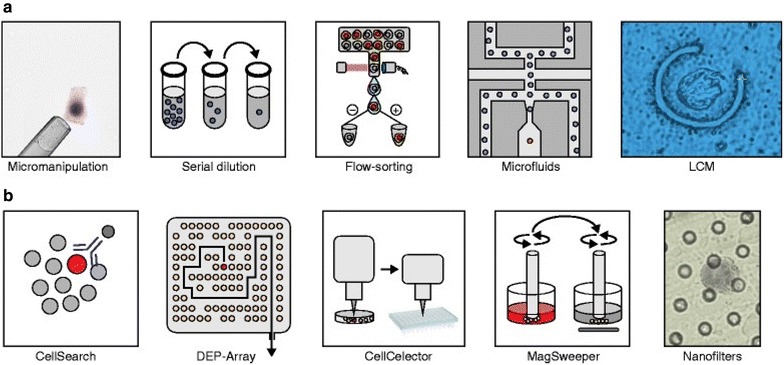


显微操作技术(Micromanipulation): 利用显微操作仪直接人工操作实现单个细胞的分离。显微操作仪通常由倒置显微镜和电动机械控制的微针构成 – 微针是一根具有吸头的毛细玻璃管。操作者在显微镜下寻找悬浮于液滴中的目标细胞样品,手工或通过显微操作仪将微针靠近并吸取目标细胞,然后转移至收集容器。其优点是操作容易进行,通过直观、准确地分离单个细胞,并且设备、材料成本低。但人工成本高,通量低,主要用于较小细胞群体中的目标细胞分离。并且分离过程中容易损伤细胞,且细胞识别的过程中容易出错,未来或依赖于半自动化的细胞分离设备克服这些部分不足。
梯度稀释法(Serial Dilution): 将细胞进行梯度稀释,最终得到单个细胞。其有点很棉线,就是技术简单、成本低廉,但在分离过程中容易出现分离错误或者丢失细胞、实际的分离效率难以保证,且这种方法仅适用于样本可以培养的研究。
流式细胞仪(Flow-Sorting):待测细胞经特异性荧光染料染色后,加入样品管中,经过测量区,由染色后的细胞在激光照射下的荧光产生的电信号来进行定量分析; Flow Sorting法可以测量细胞的多个特征 (比如大小, 粒度, 内外荧光等) , 且准确度、灵敏度和通量均处于较高的水平。但 需要大量的悬浮细胞作为原始材料,可能影响低丰度细胞亚群的产出;此外,仪器中快速流动的液流、及过程中涉及细胞的消化及分选等因素,可能对细胞的活性及表面标记产生影响,从而影响实验结果的准确性。
微流控技术(Microfluids):微流控技术是一种用于精确控制微量液体的技术,可以将单细胞的培养、制备、反应、分离、检测等步骤集成到一块微米尺度的微流控芯片上,自动完成分析全过程。一般基于以下三种原理: 油基液滴分离、气动微阀、流体动力学细胞陷阱技术。基于微流控的液滴生成技术是通过水溶液和油相从不同的微通道中流出并融合,形成一个 “油包水” 的乳液滴,将单细胞包被。目前市场上的代表产品有HiFiBiO的自动化细胞发现平台CelliGO以及英国Sphere Fluidics公司的Cyto-Mine单细胞分析,以及下文将提到的ICELL8、 BD Rhapsody等。微流控技术成本低,消耗样本及试剂少,在提高效率的同时也防止了样品的污染。
激光捕获显微切割(LCM):LCM技术可以在显微镜直视下快速、准确获取所需的单一细胞亚群,甚至单个细胞,其基本原理是先将样本放入冰冻切片机中处理,之后通过激光束使覆盖于组织切片上的透明膜熔化,在直视下选择性地将目标细胞或组织碎片粘到该膜上,从而实现细胞分离。冰冻切片的制作是 LCM 技术中关键的一步,其质量的好坏直接影响 LCM 对目标细胞的 捕获及后续试验结果的准确性。LCM基本不损伤组织结构和待测细胞周围组织的形态完整,可以把控待测样本的质量。但用这种技术来获取单细胞的花费高、许多时候切割不够精确,且UV对DNA/RNA可能造成一定程度的损伤甚至丢失细胞核遗传物质。
以上提到的单细胞分离方法并不适用于对稀有单细胞的研究。现在,已经开发了几种新技术来弥补上述方法在稀有单癌细胞分离中的缺点,例如CellSearch (强生),MagSweeper (Illumina),DEP-Array (Silicon Biosciences) CellCelector (Automated Lab Solutions) 和Nanofilters (CellSieve)。
CellSearch™:是目前唯一获得FDA批准的细胞分离系统。该系统的重要组成部分是CellSearch®上皮细胞试剂盒,该试剂盒包含磁性捕获颗粒,其表面层覆盖有靶向上皮细胞的抗体,可以捕捉血液种的CTC。和颗粒结合后的CTC能够和未结合的细胞在磁场的作用下,发生分离。 此系统已应用于医院中转移性前列腺癌,乳腺癌或结直肠癌患者的监测。
DEP-Array™:此系统结合了大小和细胞表面表达特性进行细胞分离。 DEP-Array™通过密度梯度离心以及抗体染色来实现目标细胞的富集,然后使用微流控芯片分离单个细胞。
MagSweeper™:是一个自动化系统,还使用免疫磁分离来纯化循环中的稀有细胞。磁棒被自动扫过包含来自外周血中标记细胞的样品,以特异性捕获循环的上皮细胞。连续几轮的细胞捕获-洗涤-释放-重新捕获导致上皮细胞富集108倍。
CellCelector™:是一种使用自动微操作从密集的单细胞微阵列中分离单个细胞的技术。来自培养物(或外周血)的细胞悬浮液沉积在包含微孔的定制阵列上,阵列上覆盖有单克隆抗体。使用微阵列扫描仪,可以定位目标细胞,然后通过机械臂从微孔中取出单个细胞进行后续分析。
Nanofilters: 此系统可以根据大小区分而不是特定的细胞表面标记物来捕获各种循环中的肿瘤细胞。
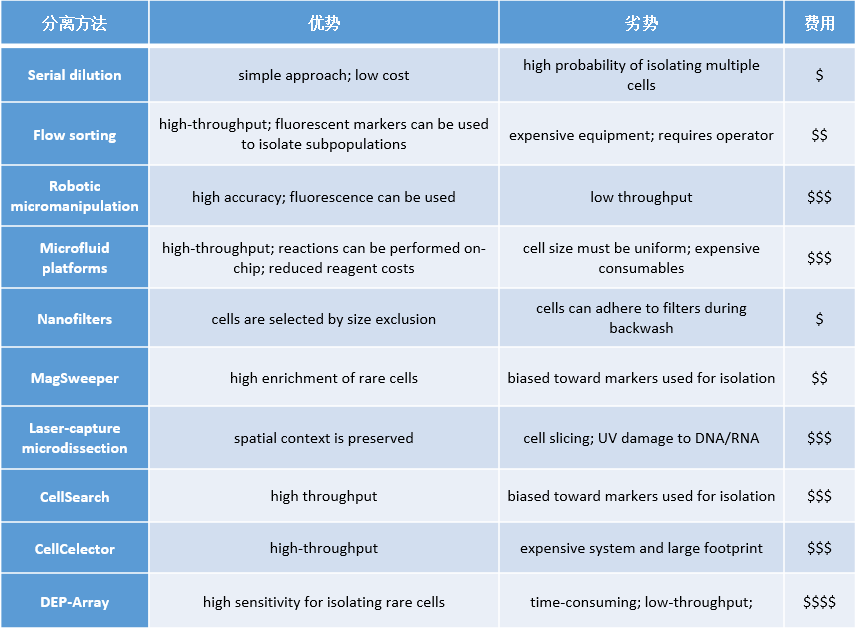


▲Mol Cell. 2015 May 21; 58(4): 598–609.
5.产业链核心玩家的技术PK
单细胞测序行业分布与整体测序行业分布相似,上游包括提供检测设备和试剂公司。中游是将测序技术应用于临床或者研究的公司,是测序设备和试剂的使用者。下游企业主要是第三方中介服务类型公司。由于进入门槛低,中下游测序服务不掌握成本话语权,竞争异常激烈,光国内相关企业就有600余家,不同公司侧重点不同,基本可以划分为测序服务综合、基础科研、临床应用、生信分析和个性化健康管理方面,其中以涉及临床的企业居多。
上游垄断行业命脉,因此对于上游的布局将是未来在市场中占据领导地位的关键。本文将重点阐述。先从海外生态圈开始。这些年来来,各大企业都在试图通过实现各个角度的创新来加快单细胞测序的市场化进程。比如Illumina以及Bio-Rad提供了可扩展的试剂盒,用以分析不同起始数量的细胞;10x Genomics专注在试用一种仪器来实现同时测量基因组,外显子组,转录组等各种测序,而BD和MissionBio则专注在涉及针对目标RNA/DNA测序的定制面板。 Nadia Innovate, Dolomite Bio 以及Royston在开发完全可控的单细胞参数。 另一方面,Fluidigm试图找到低通量的解决方案,并提供一体式的仪器,Takara的ICELL8不但可以分析大量的细胞,并且还可以实现可视化,提供从种选择一部分细胞进行下游分析的机会。 单细胞测序市场中常见的一种战略就是合作或者并购,以扩大其产品组合并加强其在行业中的地位。 Illumina公司与Bio-Rad Laboratories公司之间的合作伙伴关系就是领先企业实施此类战略的一个例子。
(A) 高通量:一般采用微流体芯片,可以和现有的测序仪器无缝衔接。虽然可以实现一体式及高通量,主要缺点是相对较低的RNA捕获效率,对抑制剂的敏感性,液滴的易碎性。因为起始细胞数高,有可能会堵塞芯片或者存在每个液滴有两个细胞的可能性。
* Chromium Single Cell Gene Expression Solution
2016年10x genomic公司推出Chromium Single Cell Gene Expression Solution平台,该平台可通过快速高效的单细胞标记、测序和分析,对复杂细胞群体进行深入细致分析,绘制大规模单细胞表达图谱。10x Genomics在2017年、2018年营收分别为7108万美元、1.46亿美元,2019年上半年营收为1.09亿美元,2018年同期为5915万美元。10X Genomics在2018年完成两笔重大的公司收购业务,分别是专注于表观遗传学的Epinomics和二维基因表达技术开发商Spatial Transcriptomics,这两笔收购业务巩固了10X Genomics在基因测序行业的地位。
Chromium平台利用微流控技术进行单个细胞分选。从横向孔道中逐一输入凝胶微珠,第一纵向孔道输入细胞,凝胶微珠与细胞碰撞后会吸附在凝胶微珠上,并通过微流控技术,将之输入到第二纵向孔道,即油相孔道中。这时候,就形成了一个个油滴输出并收集。每一个油滴中会落入一个细胞以及一个凝胶微珠,凝胶珠溶解,细胞裂解释放mRNA,通过逆转录产生用于测序的带条形码cDNA;液体油层破坏后,cDNA后续进行文库构建,使用Illumina平台对文库进行测序检测,即可一次性获得大量单细胞的基因表达数据。每个芯片有8个样品,10-20分钟内自动完成多至80,000个细胞的捕获。
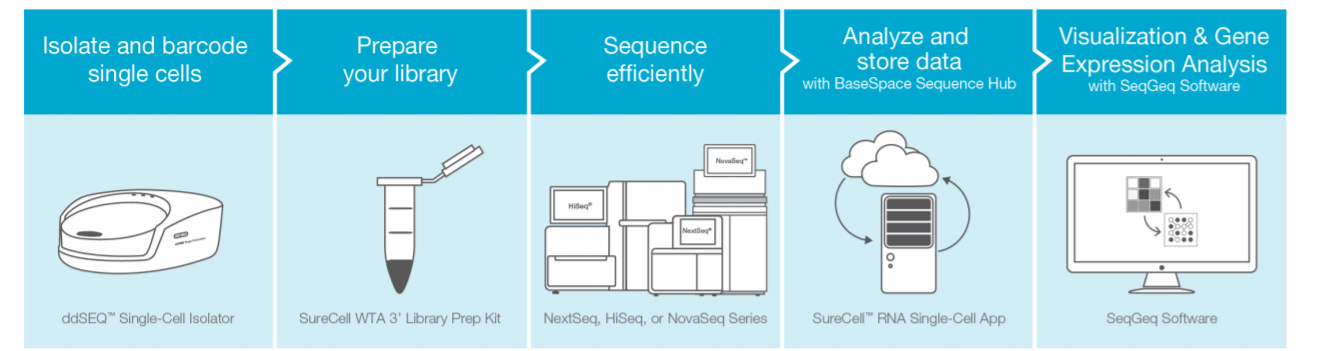
* Illumina® Bio-Rad® Single-Cell Sequencing Solution
2017年1月,Illumina和Bio-Rad发布了Illumina® Bio-Rad® Single-Cell Sequencing Solution。它借助Bio-Rad的Droplet Digital™液滴分离技术,对单个细胞进行隔离和编制条形码,然后合成cDNA。 合并并溶解液滴后,用Illumina试剂盒制备cDNA文库。 液滴在一次性药筒中制备,最多可容纳8个样品。然后在Illumina NextSeq500仪器进行下游测序,从而获得单个细胞表达谱数据。
此平台提供了可用于不同起始数量细胞的可扩展试剂盒(一种试剂盒格式可处理数百至数千个细胞,一种试剂盒格式可用于需要分析多达数万个细胞的项目)。该系统还可以使用BaseSpace® Informatics Suite,在Illumina的云端基因组学计算环境中进行初级和中级数据分析,并使用流式细胞分析技术的领先公司FlowJo所开发的SeqGeq™进行高级数据分析和可视化处理。
* Rhapsody™ Single-Cell Analysis System
BD公司2017年9月推出这款Rhapsod™单细胞分析系统:细胞悬液经注入孔注入,自然沉降到反应孔中,随后,磁珠同样由注入孔注入,即可在单个反应孔中捕获其中的细胞。平台采用的是CytoSeq特有的蜂窝板技术。该技术用20万+的微孔(该数量级远大于起始细胞数量),因此避免了Chromium种存在的概率碰撞影响捕捉效果的问题。裂解捕获的细胞,并将mRNA结合至磁珠。收集磁珠,并准备在单个试管中进行文库制备。裂解之前,先扫描阵列,然后获取有关每个样品中细胞,双峰和空孔数量的信息。它可以帮助用户确定有多少个珠子最适合文库制备,以及样品的质量是否足以进行下游分析。剩余的珠子可以在低温条件下保存3个月供后续试用。


每个细胞也会被标记特异性细胞标签,使得高通量平行建库成为可能。结合Rhapsody特有的单细胞分离技术,单次实验可制备100-10000个单细胞文库,用户可根据需求定制引物,该方法在文库制备中仅扩增目标转录本。这样将检测范围集中在目标基因,一方面可以大幅降低后续测序成本,另一方面可以提高灵敏度,并有可能检测全转录组分析可能遗漏的稀有分子。此外,提供了生物信息学管道和可视化工具,以使没有经验的用户也可以分析和理解单细胞数据。
* Nadia和RNA-Seq系统(Dolomite Bio)
Dolomite Bio成立于2016年,2017年11月推出了名为Nadia的RNA-Seq系统的新版本:单个细胞被单个珠子封装,单个珠子的表面被含有UMI序列的捕获寡核苷酸所覆盖。和其他的平台相比,这种液滴不含有进行反应的试剂,其cDNA的合成是在珠子破裂后进行,可以有效的避免小体积反应试剂的抑制作用,但弊端就在细胞捕获效率较低,最多生成48,000条带条形码的单细胞mRNA库。该芯片包含细胞和珠子搅拌器,可确保整个运行过程中单个细胞和珠子的均匀分布。该仪器专用于RNA-Seq应用,尽管其他应用也是可能的(例如DroNc-Seq或PCR激活的细胞分选(PACS)。同时也给客户提供升级到Nadia Innovative的机会。这是一个可移动的模块,允许用户开发新的单细胞方案和应用,使用自己的试剂并其他相关改动。



* InDrop系统(1CellBio)
1CellBio是哈佛大学的一个分支机构,于2016年6月启动了对其高通量仪器InDrop System的早期试用,其原理和上述平台类似:首先将细胞用携带UMI条形码引物的水凝胶微球包裹,然后用裂解缓冲液和反映试剂包裹。封装后,通过紫外线释放引物,并在每个液滴中合成cDNA。然后将液滴打碎,并扩增所有细胞中的物质以进行测序。一个芯片可以有六个样本,可对40,000个细胞进行条形码编码,声称细胞捕获效率高达90%。2019年4月宣布可以向特定客户提供其专有的inDrop™水凝胶珠粒,该珠粒由针对用户定制的引物合成。此外,价格也是一大优势,每个结果大概是5美分/细胞。 2018年,有多篇顶级刊物上发表的文章都是试用此系统。
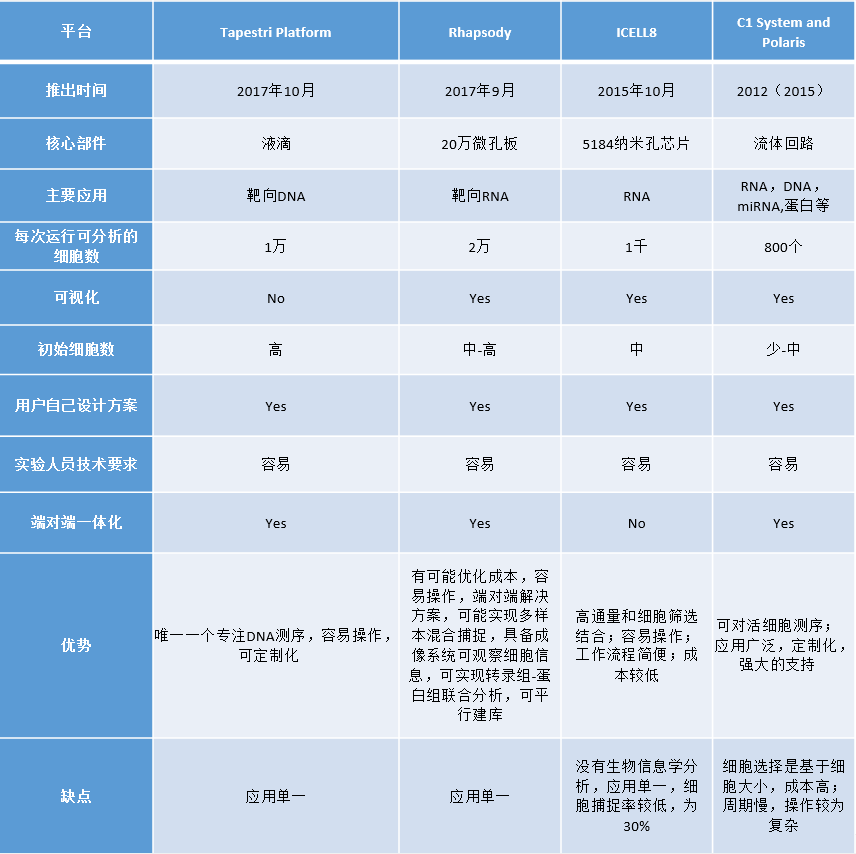
* Tapestri平台(MissionBio)
与上述仪器不同,MissionBio的Tapestri平台(于2017年10月推出)的主要应用是靶向DNA-Seq,很适用于需要有关单个单细胞中突变的信息时,因此在免疫学和肿瘤学的精确医学中非常有用。仪器分为两步工作流程。第一步,将细胞与蛋白酶混合,形成单个液滴。然后在标准的热循环仪中进行细胞裂解和蛋白酶消化,使DNA可用于后续扩增。然后将含有细胞裂解液的小滴重新装入仪器中,并与条形码小珠和试剂混合,以扩增特定区域。该平台一次运行最多可分析10,000个细胞。该公司提供了定制具有目标靶点的单细胞突变图谱的可能性,其中可以同时分析多达100个基因组区域。
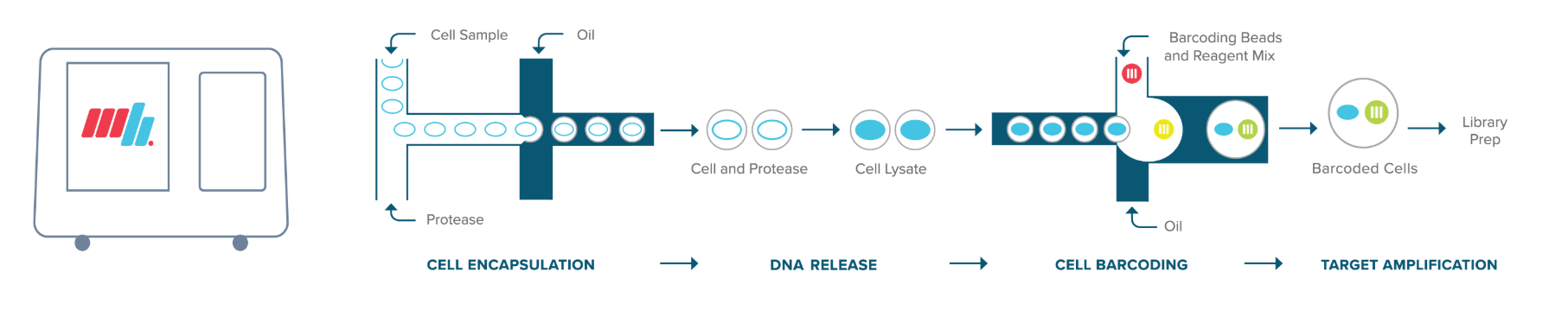


(B)中通量:它们结合了自身的优势,提供足够的通量以允许大规模研究调查细胞异质性,但重点是通过视觉控制选择的狭窄亚群。 这降低了测序成本,生物统计学分析的难度也降低了。
* ICELL8 Single-Cell System
2015年2月份,Wafergen公司开发出ICELL8 Single-Cell System单细胞分选平台,该平台具有通量高,周期快等特点,解决了传统单细胞扩增中通量低,价格贵的问题,为需进行大量细胞捕获筛选的研究提供了高效单细胞分选平台。ICELL8单细胞系统于2015年10月启动,是一种独特的仪器,将高通量与可视化控制和主动选择感兴趣的细胞用于下游RNA-Seq分析相结合。该仪器是WaferGen多样品纳米分配器(MSND)与强大的成像站的结合。第一步,MSND将带有试剂(通常为50 nL)的细胞分配到带有预打印条形码的5184纳米孔芯片中,最多可捕获1907个单细胞,然后在15分钟内分配8个样品,特殊配制的稀释剂以及对温度和湿度的环境控制有助于在整个细胞分离过程中维持细胞活力。分配后,成像站扫描芯片,然后选择感兴趣的细胞进行分析。可以使用SCRB-Seq方案结合Nextera XT DNA库制备试剂盒(Illumina)来制备测序文库。也可以使用与使用的条形码兼容的其他方法。通过这种方法,一天可以处理多达15,000个视觉选择的细胞。Wafergen于2016年被Takara Bio收购。
* C1™ 单细胞全自动制备系统
Fluidigm公司是单细胞测序的开辟者,从2012年推出C1后经历了一系列的改革。C1与BioMark™ HD微流体PCR系统相结合,能够快速可靠地分离、处理、并对单一细胞进行基因组分析。 C1单细胞自动制备系统微流体技术,可以同时捕获96个的细胞,在同一张芯片上完成细胞捕获、裂解、逆转录及预扩增的全过程。在BioMarkHD系统进行qPCR扩增,几个小时内即可检测数以百计的单细胞中数百个基因的表达,而这些工作在传统检测流程中通常要耗费几天的时间。芯片中细胞的选择基于大小,目前允许分离5–10、10–17和17–25 µm范围内的细胞。 2015年,推出了新版本的C1芯片,可处理多达800个中型单细胞(10-17 µm)。
从传统的RNA测序和靶向基因表达到全基因组和外显子组测序,靶向DNA测序,表观遗传学和miRNA表达,以及最新推出的蛋白组学,C1的应用广泛,并且提供定制化服务。另一款名为Polaris的革命性仪器于2015年推出,这是第一个也是唯一一个针对活化细胞的测序平台。
* 其他平台
其他值得关注的平台企业包括Stilla Technologies,CellMicrosystems, Menarini Silicon Biosystems, AVISO CellCelector, Angle PLC,Hifibio,Celsee,Fluxion Biosciences,Berkeley Lights等。美国Berkeley Lights(BLI)的纳米光导流体平台Optofluidic Platform是结合微流控的纳升级微反应器技术 (Nano-Pen) 、光电定位技术(OEP)以及计算机系统的一体化完成单细胞分选、分析、培养以及导出功能的多功能单细胞平台。





中国公司大部分是以测序模块为主,包括和知名制造商合作的如华大基因,贝瑞和康、达安基因、博奥生物等,少量厂家也具备自研能力,比如华因康、瀚海基因等企业。华大基因、贝瑞和康、达安基因等生产的测序仪已经获得CFDA的批准。据估算,我国约有1700 台NGS测序仪,几乎都是Illumina(约1000 台)、Thermo Fisher(约600 台)和Pacific Biosciences(约50 台)的仪器,其他的仪器只有约50台。这些企业的测序仪都可以作为单细胞测序的下游设备。
在国际上享有盛誉的当属诺禾致源,该公司于2011年3月在北京中关村生命科学园注册成立,致力于成为全球领先的基因科技产品和服务提供者。和海外企业有着紧密的合作:2015年,clontech认证诺禾致源为中国地区唯一单细胞RNA-Seq™合作伙伴;2019年7月,诺禾致源宣布携手美国基因诊断公司Mission Bio,在单细胞DNA测序领域达成深度战略合作。成果方面,诺禾致源已成功完成单精子全基因组测序、单细胞转录组测序等,结题项目有2000+, 相关研究成果在Science、 Nature等顶级科学期刊发表。其商业模式是原始设备制造商贴牌为主。
其他专注在单细胞测序的企业大部分还处在中小型规模,以下是详细信息:
晶能生物:是新开源医疗集团的全资子公司,2019年正式启动“万例单细胞全景计划”。该计划旨在基于先进的10x Genomics Chromium™技术平台,联合全国科研工作者,在单细胞水平、多组学层次,全方位了解生物体,为基础研究和转化医学提供切实的理论基础。2019年4月,晶能生物率先成为10x Genomics质量认证服务商,之前也是罗氏、BioNano的认证服务商。同时,该公司还引进了5台NovaSeq 6000高通量测序仪,极大提升了测序通量。
浚惠生物:由贝壳社早期投资和孵化,安龙生命科学基金领投的数千万元Pre-A轮融资。本轮融资将助力浚惠生物加快稀有单细胞临床检测产品的开发、注册和进入临床,浚惠生物的优势是开发了独特的肿瘤单细胞鉴别标志物,不仅通过细胞外部标志物、还通过内部代谢情况,从功能性上检测细胞。
汶颢股份: 专注微流控芯片的开发。
寻因生物科技有限公司:成立于2015年,专注于单细胞分选检测技术的开发及临床转化应用,自主开发了高通量单细胞转录组测序试剂盒,可加速推动单细胞测序技术的临床转化应用,已完成由德联资本投资的数千万元Pre-A轮融资。
亿康基因:曾创造全球首例阻断单基因病成功案例的美国科学院院士谢晓亮,决定将其开创性的单细胞全基因组扩增技术落户泰州,在中国医药城创办了亿康基因。亿康基因的单细胞全基因组扩增试剂盒(MALBAC®技术)能够在4小时内,从单细胞或者等量DNA中有效扩增出2-5µg的全基因组DNA。其总经理兼联合创始人陆思嘉博士是MALBAC®单细胞全基因组扩增技术的发明人。有运用该项技术成功阻断遗传病的几千个成功案列。
鹍远基因:鹍远基因公司位于中国上海及美国加州圣地亚哥,主要产品服务包括肿瘤诊断及个性化治疗、无创产前诊断等。2016年8月,成功完成2000万美金的A轮融资。本轮融资由礼来亚洲基金领投,松禾资本以及辰德资本共同投资。
新格元:成立于2018年1月,致力于开发简便可靠的海量单细胞组学技术,使之成为新一代分子诊断工具。 现已有十余项核心技术的专利申请及软件著作权,并于2019年1月推出国内首款海量单细胞测序产品——新格元GEXSCOPE™海量单细胞RNA测序产品。产品包括自主开发的微流芯片,所有配套试剂以及生物信息分析软件的整体解决方案。迄今为止,新格元生物总融资已超过1亿元人民币,由夏尔巴投资领投,华创资本及天使轮投资方元禾原点及峰瑞资本跟投。
怡天生物:则采用液体活检技术,自主研发了两个创新的专利技术来分离细胞,既能保证细胞完整和活性。也可以高准确度的(90%以上)分离出纯度100%的单颗肿瘤单细胞。这两个专利技术平台分别是A+QT系统和A+SCDrop系统。A+QT系统运用可量产的微流体晶片技术来捕获血液样本中的少量肿瘤细胞,可在35分钟内将5mL全血中的CTC以免抗体无损细胞活性的方式高效地筛选出来,移除99.99%的白细胞。该技术已做到全自动化运行。A+SCDrop系统是利用油包水的乳化技术结合高速细胞介电特征分析技术,可将A+QT富集后的产物样本,分成数百万颗0.1 nL的极小液滴,由于全血经A+QT富集后的样本仅剩CTC与数万颗WBCs,因此每颗小液滴中最多仅会存在一颗细胞。此平台相关技术已申报13项国内外专利。
杉米科技/净信:净信的单细胞测序仪每个样本能够产生5000~10000个细胞,对上机样本没那么多的要求。为减少实验失败造成的损失,机器还添加了能够监控实验过程的系统,一旦出现管道堵塞等情况,便可以及时止损。而关键的还是:该平台不论是从机器的购买成本,还是试剂耗材的成本都较低。
万乘基因:万乘基因成立于2018年,已建立好了具备100%全自主知识产权的高通量单细胞转录组测序技术平台,包括设备、芯片、试剂和分析工具等,主要业务是利用自主研发的高通量单细胞测序技术平台服务于科研、临床以及工业市场。现阶段,已和十家顶级三甲医院开展合作,提供单细胞技术服务,且已有成果发表于Protein & Cell杂志。据悉,该成果是国内发表的首篇使用非10x Genomics技术的高通量单细胞转录组测序平台进行研究的论文,初步证明了该技术平台的稳定度。2019年获得500万元天使轮融资,投资方为合力投资。
浚惠生物:成立于2015年,创始人阎灼辉为单细胞检测仪器专利联合发明人,有20多年跨国企业、民营企业管理经验。公司主要在单细胞的自动分离和单细胞鉴别两个方面实现了突破,已经开发出来了单细胞自动分析仪,分离一个单细胞用时在1秒钟左右。在临床中一天可以完成30-40个检测,达到了常规检测水平,走在了临床应用转化的前列。在单细胞鉴别上浚惠生物也有独特的鉴别方法,不仅看细胞外部标志物还看内部代谢情况,从功能性上检测细胞。而扩增这个步骤,浚惠生物选择和行业最佳的WGA(单细胞DNA扩增)技术产品有合作。目前其仪器和针对肿瘤的检测试剂都已经开发完成,正在准备申报医疗器械注册证。浚惠生物近期已获得华大专注于天使投资的奇迹之光基金千万级投资,在此之前,浚惠生物还获得贝壳基金天使轮投资。
中科纳泰:就是一家专注于液体活检中CTC技术的研发型企业,由中科院国家纳米研究中心的胡志远、杨延莲、方巧君、王浩四位海归博士共同开发,拥有五个国家级实验室的团队。中科纳泰采用的是第二代生物法技术,通过高特异性多肽包裹纳米磁珠,由外部磁场的吸引,捕获在外周血中的循环肿瘤细胞。第二代生物法相比于第一代物理法准确性更高,可以达到95%,这也是公司的核心优势之一。2016年完成4000万元的Pre-A轮融资,投资方包括中国平安和硅谷投资等。
6.瓶颈及挑战
细胞活性的保持:现有的分离过程会诱导意外的细胞应激,从而改变细胞的行为,活力和特性,使其不处于自然状态,所以急需新技术以柔和的方式分离细胞,确保其活性。其中一个方向就是利用皮微滴技术(picodroplet)的细胞打印机和微流体平台,比如Cyto-Mine®单细胞分析系统(Sphere Fluidics)。随着技术的发展,下一级别的分析会朝着在组织的背景下进行分析的方向发展。
细胞分离及捕捉:现有大部分平台是基于微流体技术的,因为很容易集成到下一代测序管线,然而这些工具往往会受到捕获效率的限制 (高至65%,低至3%)。在这种情况下,稀有细胞群很可能会丢失。还有另一个阻碍是现有的平台需要大量的原始细胞,这个方面也需要有新的技术来进行改良。
扩增:一个单细胞中所含的DNA/RNA量少,现有的基因测序都要先进行扩增,而在扩增复制的环节容易出现复制错误或者丢失的情况。
工作流程:可以从几个方面进行优化:1)尽管对多种分析物(DNA,mRNA,调节性RNA,蛋白质,代谢物)的测量对于描述细胞的复杂性将具有更大的价值,但目前大多数用于单细胞分析的方法提供了仅分析一种分析物的可能性。在单个细胞上执行多个测定或连续评估单个细胞的灵活性,可以洞察其动态变化。一个例子就是,BD宣布升级其Rhapsody仪器以允许蛋白质检测;2)开发强大的自动化工作流程以提高准确性并减少必要的动手时间;3)开发用户友好的分析工具,利用人工智能检测数据趋势、区分异质种群中的生物噪声等。在这一领域,瑞士初创公司Scailyte正在开发一种基于AI的解决方案,以从单细胞数据中发现生物标记,并在短短几个小时内分析复杂的数据集。美国初创公司Cellarity也在这一领域开展工作,力求将单细胞测序与人工智能和CRISPR基因编辑相结合。
费用:单细胞测序的使用受到限制,部分原因是其成本高昂。 所需的大多数仪器和试剂都很昂贵。 例如,如果希望将单细胞测序整合到实验室中,10X Genomics的仪器售价约为5万美元。 一个典型的运行,包括细胞分离和测序,每个样品的成本在3千-1万美元。美国Mission Bio公司正在着手解决这个问题,旨在将典型运行的成本降低到1,000到2,000美元之间。此外,将富集技术与高通量单细胞分析仪器合并的趋势非常明显,能够主动选择以高通量分析的定义的细胞群,将减少分析的细胞数,大大降低实验成本,并且下游生物信息学分析将变得不那么复杂。
知识产权:在任何具有巨大市场潜力的地区,知识产权都会引起冲突,这可能会对新技术的发展产生负面影响。 例如,早在2015年,Bio-Rad起诉10X Genomics侵犯专利,陪审团裁定它必须支付2100万欧元的赔偿金。 此外,10X Genomics无法将其产品销售给新客户,因此仅限于为“历史客户”提供服务,所有过去和将来的销售均需支付15%的专利使用费。几个月后,美国公司Becton Dickinson也起诉了10X Genomics。 之后,该公司决定建造新设备以增强其知识产权地位。
参考资料:
Nat Rev Genet. 2013 Sep;14(9):618-30.
Front. Cell Dev. Biol., 25 October 2016
Mol Cell. 2015 May 21; 58(4): 598–609.
Clin Transl Med. 2017; 6: 15.
Clin Transl Med. 2017; 6: 10.
Cell Biosci. 2019; 9: 53.
Front. Cell Dev. Biol., 25 October 2016
Nature Protocols volume13, pages599–604 (2018)
https://doi.org/10.1146/annurev-biodatasci-080917-013452
https://teichlab.github.io/scg_lib_structs/
doi: https://doi.org/10.1101/541433
Int. J. Mol. Sci. 2018, 19, 807
Ellsworth et al. Clin Trans Med (2017) 6:15
Brief Funct Genomics. 2019 Mar; 18(2): 119–128.


评论