2020年1月12日,J.P.摩根医疗健康大会期间,以“聚焦中国机会,促进跨境合作”为主题的对接会议China Focus®也将同期开幕。作为JPM周的热身会议,China Focus®也是聚焦中国系列规模最大的盛会,预计600参会人,200中方企业,300项目,600+一对一会议。
China Focus®是专注医疗健康跨境投资与合作的系列会议,旨在为海内外创新项目、企业和投资人搭建跨境合作的高效交流平台,分享中国和海外市场的创新、资本、商业和政策前沿资讯,交流跨境合作经验,最终建立合作。自2019年以来,China Focus®已在美国旧金山、维也纳、费城、波士顿、汉堡等全球生物医药创新城市举办,吸引了超过600多家中外企业、1000余[X1] 位高管参与,成为关注中国与海外跨境合作最重要的品牌活动之一。
跨境项目对接是China Focus®最主要的特色服务之一,在每次会议筹备期间,主办方会从全球各地筛选并邀请有兴趣进入中国市场或与中国企业合作的创新项目参会,为中国企业提供项目咨询、预对接的服务,帮助中国企业做好准备,在会议当天与项目方高效对接。
本次China Focus®@San Francisco,我们征集了300+的海外项目,面向有参会ChinaFocus®意向的中方企业开放。全部项目将分4期进行推送,如果您对其中的某些项目感兴趣,可以联系我们。
* 早鸟报名福利(11月29日前付费报名有效)
• 150美金报名优惠
• 30分钟电话咨询服务:会前深入了解您的参会需求,根据您的需求定向邀请项目
• 获得项目BP:您可以获得10个感兴趣项目的BP
• 预对接服务:会前三周(12月23日-1月12日),我们会根据您的需求为您定向推送参会项目,并协助您预约会议现场的“一对一”对接会议
• 现场对接支持:在会议现场,我们的工作人员将支持您高效地与预约好的企业进行“一对一”对接
*项目详情
抗体
1、项目T128:用于治疗心脏病的全球唯一的利用DNA配体消除自身抗体的临床期产品
项目背景:研究表明自身抗体和肾上腺素受体的结合可导致80%的扩张型心肌病患者心脏细胞死亡和器官衰竭。靶向β1肾上腺素受体的自身抗体可通过称为免疫吸附的复杂血液清洗程序后被消除,并可显著改善心脏功能。接受免疫吸附后5年,患者的生存概率比未接受免疫吸附的患者高43%。但这种血液清洗非常昂贵。
T128这是一种能结合并消除靶向β1肾上腺素受体的致病性自身抗体的DNA配体(Aptamer)。在一项I期临床试验中,单剂量静脉输注此药物能完全和可持续地消除靶向β-1肾上腺素受体的自身抗体。并具有极好的耐受性及安全性。已经启动临床II期。
公司介绍:一家私人控股公司,成立于2014年,总部位于瑞士楚格。其核心研发团队是来自MaxDelbrückcenter、CharitéBerlin和柏林德国心脏研究所的科学家,有着超过10年的研究自身抗体的经验。首次发现自身抗体便是来自MaxDelbrück center的成果。
产品优势:
• 全球唯一的利用DNA配体消除自身抗体的临床期产品
• 和血液清洗比较有绝对的价格优势
• 无毒及无免疫原性
• 非常高的稳定性,方便运输
• 动物试验中显示了良好、持久的消除自身抗体的能力 (180天)
• 有治疗治疗肺动脉高压,青光眼等广泛潜力
2、项目T320:一个诺贝尔奖委员会成员创立的肿瘤免疫疗法的多特异性抗体企业寻求融资合作
项目背景:多特异性抗体用于肿瘤免疫疗法近几年来得到了制药行业的广泛关注。不同于单克隆抗体, 多特异性抗体能够同时与两个或者多个抗原结合,从而增强特异性,提高对肿瘤的杀伤。安进公司的Blinatumomab是美国FDA目前唯一批准的针对肿瘤的双特异性抗体,用于复发性急性淋巴母细胞白血病的治疗。另一获批的Emicizumab是靶向凝血因子IX和X,治疗A型血友病。
除安进外,罗氏、礼来、GSK、强生等大型制药公司也纷纷布局。中国目前有包括恒瑞、友芝友生物制药、信达生物、上海岸迈生物和正大天晴等在内的超过15家公司参与双特异性抗体的研发。2019年2月,正大天晴与美国Abpro 签署了一份最终价值可高达40亿美金的双特异性抗体开发合作协议。同年六月,上海岸迈生物获得7400万美金的B轮融资使其总融资量接近一亿美金。
虽然多特异性抗体的开发平台众多,但是其产业化仍面临着来自血液半衰期、抗体稳定性和表达量、纯化及下游生产等诸多方面的挑战。而项目T320提供了一个可以解决以上挑战的快速可控的多特异性抗体研发平台。
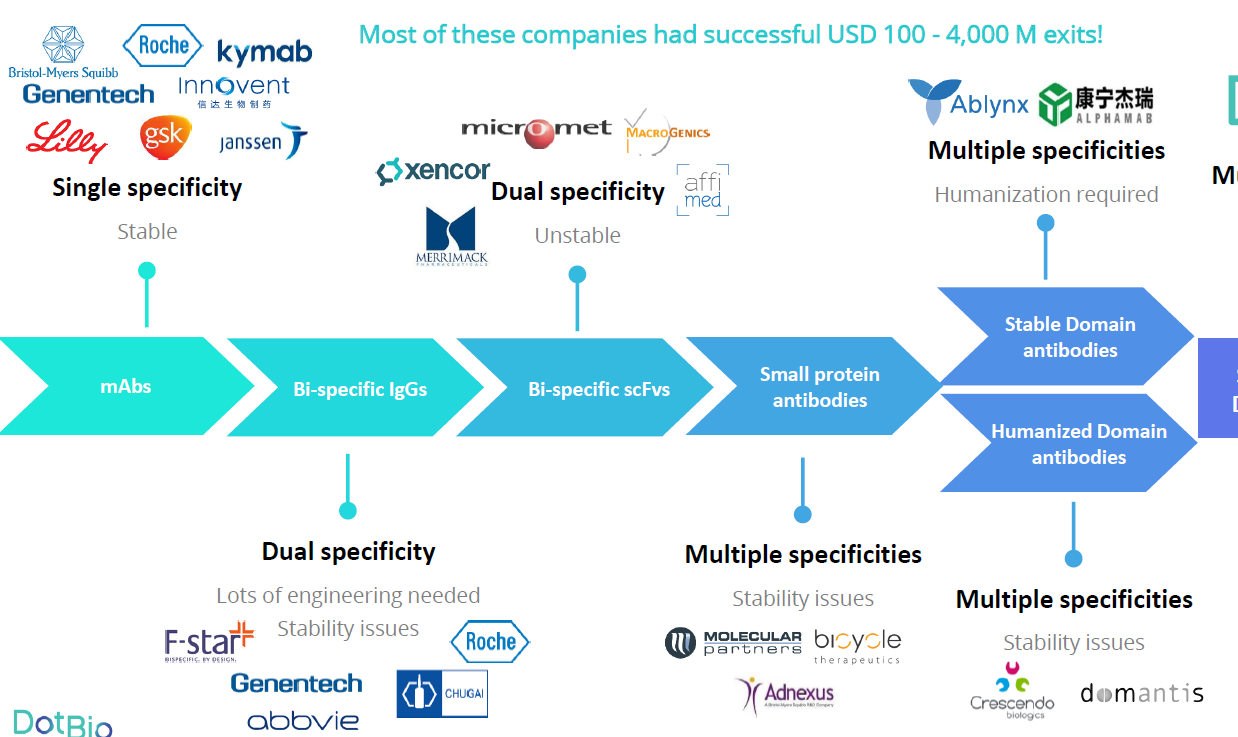


公司介绍:一家位于新加坡的专注于肿瘤免疫多特异性抗体的临床前公司。公司创始人是诺贝尔奖委员会成员,瑞典皇家科学院院士,和一名持续创业者。公司基于专有的噬菌体抗体展示,抗体稳定化筛选,以及模块化组装技术可以在12个月内生产出稳定高表达的人源化多特异性抗体。公司现有四个临床前候选多特异性抗体用于实体肿瘤的治疗,其靶点覆盖免疫检查点如PD1/PDL1及肿瘤靶向抗原如Her2。
平台优势:
• 灵活的模块化抗体组装平台可以控制靶点数量、类型及结合强度
• 快速筛选稳定化抗体保证了产业化生产的可靠及可控性
• 可根据临床需求简单快速的添加效应功能及提高抗体的血液半衰期
• 12个月可以完成抗体生产
• 技术具有很强的专利保护性
3、项目T345: 同类第一抗体-配体复合药物针对PD-1抑制剂难攻克人群
项目背景:抗体 (antibody)和核酸适体 (aptamer) 是两大重要的生物制剂。2018年,全球抗体市场规模高达1232亿美元,其中罗氏、艾伯维、强生、诺华、安进等在内的七家制药巨头年销售额高达50亿美元以上。近几年来,多特异性抗体更是得到了制药界的广泛关注。除安进外,罗氏、礼来、GSK、强生等国际大型制药公司,中国目前有包括恒瑞、友芝友生物制药(YZY Bio)、信达生物(Innovant)、上海岸迈生物(EmpimAb)和正大天晴等在内的超过15家公司参与双特异性抗体的研发。核酸适体目前的研究不仅包括作为治疗黄斑变性、癌症、及糖尿病等疾病的药物,同时也在诊断和靶向药物输送有着广泛的应用。然而,抗体和核酸适体的开发依然面临很多挑战比如稳定性和体内的血液半衰期。项目T345提供了一套可以快速高效筛选及开发抗体和核酸适体的技术平台。
公司介绍:一家位于波兰处于临床前期同时具有抗体和核酸适体自主研发和合同外包服务的生物制药上市公司。公司共有两个临床前治疗癌症的抗体药物及两个基于核酸适体的血液单采技术。
产品及平台优势:
• 两大自有技术平台可快速高效的筛选合成抗体和核酸适体
• 同类第一的免疫配体-抗体复合体可以同时抑制癌细胞生长及调节相关的免疫反应,一方面可以将冷肿瘤转化成热肿瘤,另一方面因为基于和PD-1信号通路不同机理,有潜力针对更为广阔的市场
• 基于核酸适体的血液单采技术可以提高该技术的安全性,并有效移除过滤血液中的致病因素
• 公司具有九年以上的研发经验,已完成超过170个研发外包项目,具有高性价比且完整的生物药物开发平台
4、项目T333: 下一代口服给药的单克隆抗体类似物
项目背景:自从1986年全球首个单克隆批准上市以来,经过30多年的发展,抗体药物已成为全球生物制药增长最快的细分领域。2018年,全球抗体市场规模高达1232亿美元,其中罗氏、艾伯维、强生、诺华、安进等在内的七家制药巨头年销售额高达50亿美元以上,艾伯维的阿达木单抗更是上市16年来的累计销售额达1319亿美元。然而,抗体药物依然具有不少的局限性比如免疫原性和体内组织穿透性。不仅如此,抗体生产成本高昂并且很难用于口服治疗。项目T333通过全新的组合化学设计和高通量筛选可以合成出靶点亲和力强,特异性高,无免疫原性、可用于口服给药的下一代抗体类似物。
公司介绍:一家处于临床前阶段致力于开发全新一代抗体类似物的生物制药公司。公司目前筛选的靶点涵盖肿瘤免疫、阿尔茨海默、艾滋病等多个治疗领域。
平台优势:
• 抗体类似物能抵抗肠道内的蛋白消化酶,可用于口服治疗
• 通过组合化学平台可加入D型氨基酸从而消除抗体类似物的免疫原性,提高安全性
• 生产成本便宜,产量可在吨级
• 更好的组织穿透性,提高抗体类似物的疗效,还可用于多种给药途径
• 公司的平台技术具有很强的专利保护性
细胞治疗
5、项目T158:一款用于治疗肝癌且仅为现有治疗费1%的即用型CAR-T疗法
项目背景:诺华旗下的CAR-T产品Kymriah 以及Gilead旗下的Yescarta获批后销售均不及预期。这种近五十万美元的高昂价格显然限制了其市场潜力,尽管医保方面正在做努力,也提出了Pay-for-performance的尝试,但若要从根本上解决问题,还是需要降低成本。
在这大背景下,“即用型(off the shelf) ”CAR-T的概念应运而生。“即用型”CAR-T是将健康供体的T细胞,通过一系列基因改造和扩增,使其能通用于所有病人的新型细胞制备技术。和传统的CAR-T比较,这一技术大大简化了CAR -T细胞生产的周期和成本,也能达到大规模的工业化生产以及标准化的质量控制,保证了不同批次产品之间质量的稳定均一。Cellectis是最早开始布局“即用型”CAR-T的公司之一,其临床试验UCART19公布的83%的完全缓解率与诺华的Kymriah用于报批FDA的数据完全一致。
T158是一款针对亚洲流行癌症类型-肝癌的即用型CAR-T。
公司介绍:是一家私人以色列细胞免疫肿瘤学公司,正在将一种新型免疫治疗技术推向晚期临床开发。同时也新成立了美国子公司,负责推动从目前的IIA期临床开发阶段到商业化的进展。此公司与美国MD安德森医疗中心、泰国的Khon Kaen Medical Center、以及曼谷的Thammasat大学和Chulalongkorn大学一起合作临床II期试验。
产品优势:
• 全球200+专利保护
• 无需组织类型匹配,一个健康个体捐赠的细胞可供750个病人进行治疗
• 定价为$5,000,只有现有CAR-T疗法的1%
• 已完成的临床试验对象为亚洲人群
• 其临床数据显示了在晚期肝癌病人中的疗效优势(如下图)



6、项目T105: 细胞治疗对抗尿毒症
项目背景:据不完全统计,国内慢性肾脏患者高达1亿人,其中慢性肾功能衰竭(俗称“尿毒症”)患者占200万,一年内新增的尿毒症患者接近30万人,加之近年来国内高血压、糖尿病的高发病率,最终都会造成肾脏衰竭,诱发尿毒症的可能性。临床显示,慢性肾脏病是一组以进行性肾损伤为特征的常见慢性疾病群,各种肾脏疾病发展的最终后果是成为终末期肾衰竭;终末期肾衰竭不仅死亡率、致残率高,且维持生存需要肾移植或透析。据统计,2014年全球用于肾脏病、尿毒症和透析治疗的费用已超过1100亿美元。目前国内透析患者总数已超过10万余人,且这个数字仅占据了需要透析病人总数的10%。预测我国每年用于透析治疗的费用已超过百亿元,是医药市场的又一亮点。
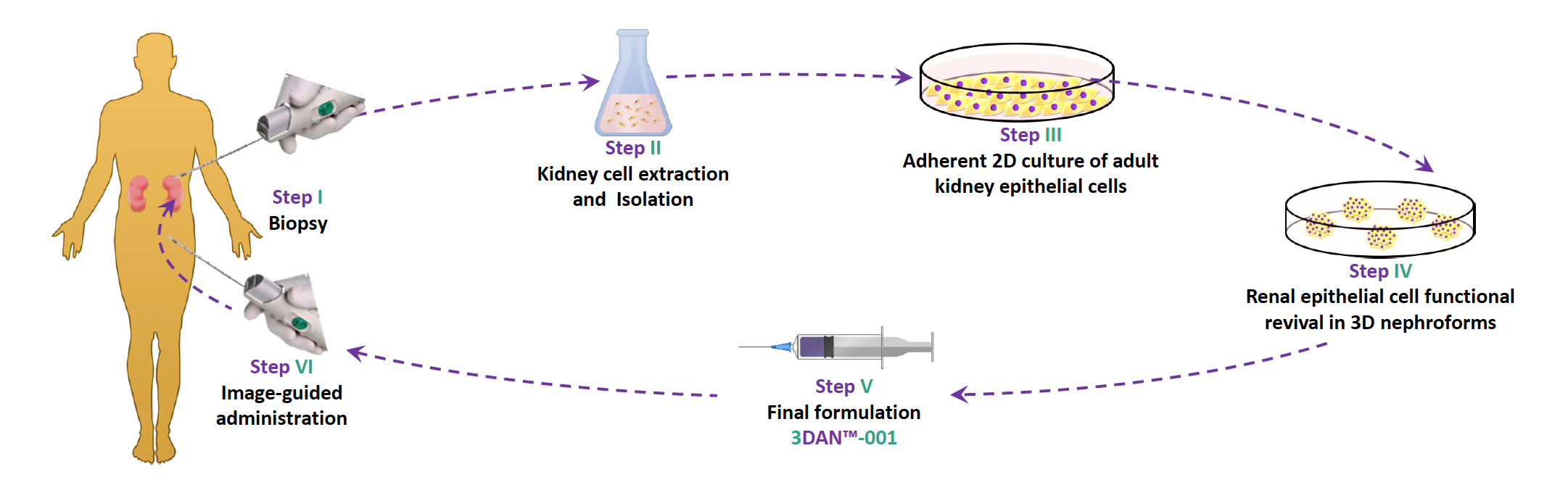
公司介绍:总部位于以色列的生物技术公司正在开发新型且专有的再生细胞疗法,用于治疗晚期慢性肾脏病(CKD)。预期这种出色的治疗方法将大大延迟对透析和肾脏移植的需求,并为CKD患者提供更长寿,更高质量和更高生产力的机会。
产品优势:
给药后,3DAN™-001疗法可减轻炎症和肾纤维化的形成,促进肾小管功能,并通过这样做显着改善肾功能。


7、项目T107: 定向分化调节性T细胞靶向阿尔兹海默症
项目背景:目前科学家们尚未找到引起阿尔茨海默氏病的病因及其机制,但已在患者的大脑中观察到老年斑和神经原纤维缠结,并发现了神经细胞凋亡,突触损失,Tau蛋白变性及其形成机理。实际上,在过去的30年中,已经对阿尔茨海默氏病的病因和治疗机制进行了各种研究,并且进行了许多临床试验。特别地,在诸如阿尔茨海默氏病,帕金森氏病和亨廷顿氏病之类的退化性脑疾病中,已经在动物模型中确定了干细胞对神经细胞再生技术的治疗作用,并且神经源性炎症在阿尔茨海默氏病中也很重要。
因此,最近已经认识到通过控制神经源性炎症来预防和治疗脑部疾病的研究是重要的领域。但是,除缓解精神和行为障碍症状的药物外,仍然没有有效的治疗方法或药物可用于预防或治疗阿尔茨海默氏病。
“调节性T细胞(Treg)”是具有控制异常活跃的免疫细胞的炎症反应的特征的一种T细胞。过度的免疫反应会导致自身免疫性疾病,包括类风湿性关节炎,狼疮和牛皮癣,以及过敏性病变,例如哮喘和特应性皮炎。研究表明,通过注射受调节的T细胞可显着缓解这些疾病。因此,国内外制药公司正在竞争开发使用调节性T细胞的疗法。
公司介绍:公司位于韩国首尔,是在植物新药开发的基础上发展起来的,目前专注于治疗退行性脑疾病以开发细胞疗法。
因为对照T细胞是人体中天然产生的细胞,所以它们是安全的,并且不会分化为诸如干细胞之类的细胞,因此具有一个优点,即它们可以避免由于细胞生长不受调控而引起的癌症。同样,我们的研究人员希望,采用该技术可以分离和培养特异于阿尔茨海默氏病的靶标调节性T细胞,并将其大量扩增,从而实现高效治疗。
公司开发了一种专注于小胶质细胞与调节性T细胞之间关系的细胞治疗药物。另外,阿尔茨海默氏病药物作为植物药,目前正在韩国进行这种治疗的3期临床试验。其他植物药也有抗抑郁药和COPD的治疗方法。
基因治疗
8、项目T293:全球第一款利用外泌体(exosome)传递的III期mRNA药物
项目背景:2019年Jazz Pharmaceuticals公司和专注于外泌体疗法的Codiak BioSciences宣布达成10亿美元的战略合作,用于开发、制造和商业化针对5个靶点的候选外泌体治疗方案。外泌体是一种细胞外的膜状脂质囊泡,起着细胞间通讯系统的作用,直径只有纳米级,但可携带小分子、蛋白质、核酸等多种药物分子,并可通过工程化的外泌体精确修饰,进行特异性组织传递。项目T293便是利用外泌体作为药物传递载体,其独特之处是和有巨大应用前景的新型mRNA药物进行结合。
公司介绍:该公司的创始人包括全球第一个将外泌体疗法推到临床III期的科学家,荣获麻省理工学院卓越奖的教授,都有着丰富的科研背景。项目T293的合资企业曾经是mRNA药物领头羊Moderna Therapeutics的部门主任, 深入参与了Moderna 新一代mRNA药物发现和开发。
平台及产品优势:
• 此外泌体mRNA药物可靶向细胞内靶点,有潜力针对传统治疗手段无法解决的疾病
• 创始人将全球第一个外泌体疗法推到临床期
• 临床III期的产品在中国开启临床试验持开放态度
外泌体载体可提高组织特异性,以及降低脱靶效应
9、项目T324:一个临床阶段的肿瘤自杀基因疗法
项目背景:尽管目前仍没有美国FDA批准的上市产品,癌症自杀基因疗法(suicide gene therapy)依然是近几年基因治疗的热点。它的作用机制是通过在肿瘤细胞内表达外源性活性酶基因,可以将肿瘤周围的无毒性药物(药物前体)催化成仅对肿瘤细胞具有细胞毒性的药物,并且通过旁观者效应(bystander effect)达到杀死肿瘤细胞的目的。与传统的化学药物治疗相比,大大提高了癌症靶向性并且降低了由脱靶性毒性造成的人体损伤。然而,癌症自杀基因疗法的临床表现并不满意。大部分癌症自杀基因疗法仅能对处于分裂的癌症细胞进行杀伤而对休眠期的癌细胞或癌症干细胞无效。另一方面,自杀基因的靶向导入及旁观者效应的强弱也是限制该疗法的主要因素。项目T324通过采用全新的自杀基因疗法系统和独特的干预机制使其成为同类最好的癌症自杀基因疗法。
公司介绍:一家处于临床阶段致力于肿瘤自杀基因疗法的公司。公司的候选药物已经完成了对头颈癌治疗的I期临床,无不良反应并对晚期癌症的治疗显示了初步的有效性。美国FDA已表示如果在不设对照组非盲(single arm, open label)的II期临床中达标主要临床终点即可获批的可能性。
平台及产品优势:
• T324已获得美国FDA孤儿药认证,并有II期获批的可能性
• 获FDA拨款150万美元,用于资助斯坦福大学合作治疗10名患者
• 独特的干预机制可以对处于分裂及休眠的癌细胞和癌症干细胞进行杀伤
• 出色的旁观者效应,可在仅有0.1-1%的癌细胞转染活性酶基因的情况下,消除肿瘤
• 与个性化的分子靶向疗法相比,可适用于更广泛的癌症病人群体,不易产生耐药性,平台具有延展性,可适用于多种癌症的治疗及联合其他疗法治疗癌症
10、项目T111:靶向基因治疗特发性肺纤维化
项目背景:特发性肺纤维化是以间质性肺病知名的肺部疾病之一,广发于50~70岁年龄层。诊断使用的是高解析度CT,但无法根治。IPF是纤维化疾病最常见和最严重的形式,且预后较差,诊断后的5年生存率在15%-20%,平均生存期仅2.8年,死亡率高于大多数肿瘤,被称为一种“类肿瘤疾病”。恶性肿瘤则是威胁人类健康的常见疾病,位居人类疾病三大主要死亡原因之首,占所有疾病死因的四分之一。
纤维化的肺组织充满疤痕,机体呼吸能力逐渐丧失。众所周知,环境毒素是肺纤维化的重要起源,但是鲜为人知的是,这种疾病势必伴随着端粒损伤。不管是否出于遗传因素,肺纤维化患者的端粒都很短。当端粒变得太短时,受损的细胞就会激活“修复程序”,致使瘢痕形成,导致组织纤维化。目前唯一获批的肺纤维化治疗药物至今仍无明显疗效,因为它们的目标旨在症状,而非纤维化的根本原因。
公司介绍:公司的治疗策略是基于纠正患者肺纤维化的分子原因,即细胞端粒短,唯一有能力恢复端粒长度、修复肺组织损伤的酶是端粒酶。端粒是位于每个染色体末端的蛋白质结构,当细胞分裂时,它们保护染色体的完整性。端粒就像一顶量身定做的“帽子”,只有在足够长时才能发挥保护作用,端粒过短时,受损细胞就会停止分裂,阻止组织再生。端粒变短不仅跟衰老有关,还会导致严重疾病,例如肺纤维化。公司开发了基因治疗的方法靶向替代损伤的端粒,从而修复端粒。
疫苗
11、项目T117:突破性肿瘤疫苗
项目背景:癌症是资本的主战场,也是影响人类寿命的“头号杀手”。根据世界卫生组织的数据,2018年癌症带走了全球960万人的生命,也被认为是未来一百年内致死率最高的疾病。肿瘤疫苗可以帮助病人激活或加强自身免疫系统,从而杀伤和清除肿瘤细胞,以此来抗击癌症。它的原理是通过表达特异性的、具有免疫原性的肿瘤抗原(如多肽、DNA和RNA等),在细胞因子、趋化因子等佐剂的辅助下,激活或加强机体抗肿瘤免疫。
公司介绍:公司位于美国哥伦比亚,以研发抗癌方案为主。
产品特点:
• 新抗原疫苗
• 获得专利的平台技术(NeoAntigen Epitope NAgE发现平台)
• 鉴定高度免疫原性的细胞毒性T细胞新抗原
• 可以与任何抗癌抗体和检查点抗体结合使用
• 改善癌症免疫疗法的临床反应
12、项目T321:新一代广谱肺炎链球菌疫苗及针对传染性疫苗的开发平台
项目背景:肺炎链球菌疾病是全球严重的公共卫生问题之一,也是导致儿童和65岁以上成年人死亡的重要原因,并且抗生素耐药性问题日趋严重。中国每年有174万五岁以下感染肺炎球菌病例,居全球第二位。全球畅销的辉瑞十三价疫苗的销售额接近每年60亿美金,但仅能对28-42%的成人侵入性肺炎链球菌血清类型提供保护,并且生产成本高昂。2017年辉瑞十三价疫苗进入中国,但在1523万新生儿中仅有7.23% (约110万)的婴儿获得接种。此外,由于生产成本高,肺炎链球菌疫苗在中国仍属于二类疫苗,没有纳入国家免疫计划,需要自费进行接种。不仅如此,全球范围内也未有适用于预防所有肺炎链球菌血清类型的广谱疫苗问世。项目T321就是一家专注于研发安全有效价格低廉广谱的肺炎链球菌疫苗公司。
公司介绍:一家临床阶段致力于研发传染性疾病疫苗的公司,覆盖肺炎链球菌、脑膜炎球菌、结核杆菌、幽门螺旋杆菌和艰难梭菌等。该公司的肺炎链球菌疫苗是全球唯一的临床阶段广谱疫苗,其I期临床结果已于2017年发表, II期临床正在设计准备中。该公司与中国某医药集团签订了价值数百万美金的肺炎链球菌疫苗研发与授权协议。脑膜炎和结核杆菌疫苗已进入临床前研发后期,其中结核杆菌疫苗已授权给中国市场。
平台及产品优势:
• 和中国龙头企业达成合作协议
• 广谱,可以覆盖目前所有及可能出现的肺炎链球菌血清类型
• 多重作用机制,无需免疫佐剂,增强疫苗免疫原性,从源头消除抗生素耐药性问题
• 一期临床显示了良好的安全性
• 制造成本低廉,每副剂量小于一美金(约6.91元),远远低于其他上市或在研的肺炎链球菌疫苗,有助于市场定价及渗透
• 全球市场前景广阔,全球肺炎链球菌疫苗市场在2023年将达到105亿美金
13、项目T344:有望对抗衰老的突破性疫苗
项目背景:世界人口正逐渐步入老龄化阶段,到2050年,全世界每六个人中就有一人年龄在65岁以上以上。随着人口老龄化,中风、老年痴呆、骨质疏松、阻塞性肺病等疾病的发病人数也在不断增加。越来越多的研究表明衰老细胞(senescent cells)在这些生理过程中起着重要的作用。
2019年1月发表在Cell Metabolism的研究表明通过小分子清除衰老细胞,可以促进细胞生长及神经修复,从而缓解年迈糖尿病小鼠的多种精神疾病症状。2019年,梅奥医院(Mayo Clinics) 领导的一期临床显示清除衰老细胞的小分子在对肺纤维化病人的治疗中显示了良好的安全性及潜在的疗效。与此同时,靶向衰老细胞也得到了生物制药界的关注。2018年3月,位于美国加州湾区的生物制药公司Unity Biotechnology获得5500万美元的C轮融资(总融资量达到2.17亿美金)以推动其清除衰老细胞治疗骨性关节炎的一期临床研究。
公司介绍:一家处于种子轮阶段致力于治疗衰老相关疾病的生物创业公司。公司目前正在研发可以激发人体免疫反应识别相关抗原清除衰老细胞的疫苗平台。
产品及平台优势:
• 与目前正在研发的靶向衰老细胞的小分子不同,抗衰老疫苗有望在人体内产生免疫记忆,持久的清除衰老细胞,从而显著地降低给药频率
• 该平台可根据不同疾病的衰老细胞的抗体开发个体化疫苗,具有很好的延展性
• 中国目前65岁以上高达6.5亿,并以每年8000万的速度增长,靶向衰老细胞疗法市场潜力巨大
小分子
14、项目T183: 一款治疗胶质母细胞瘤的II期新靶点药物-加拿大上市企业
项目背景:GBM(胶质母细胞瘤)是所有肿瘤最致命的类型之一,复发率几乎为100%, 5年总生存率只有约5%。现有GBM的标准治疗手段非常有限,主要是手术,放射治疗及化疗。2011年,由Novocure开发的Optune,一种电场疗法顺利获得FDA批准,用于治疗GBM。
中国《脑胶质瘤诊疗规范(2018版)》明确申明:“目前研究显示电场治疗安全且有效,推荐用于新发GBM(1级证据)和复发高级别脑胶质瘤的治疗(2级证据)。” 再鼎医药已经获得了Optune的大中国区权益。Optune给患者带来了希望,也给Novocure也带来了$280M的年销售额,但这个仪器有将近三斤重,病人每天携带非常不方便。
公司介绍:成立于2002年的一家美国临床治疗器械公司。 该公司发明了一项突破性非侵入性设备并,可利用精确定位的超低射频能量专门调节分子和基因水平的信号和代谢途径,通过简单的方式提供治疗。该公司的CEO有着20多年丰富的产品上市及商业化的经验,CRO曾经是BMS的药物监管主任。
产品优势:
• 重量为85克
• 3个月以上的复发性GBM生存改善 (n=57)
• Optune在复发性GBM病人的中位无进展生存期为7个星期,T244为17个星期
• 150个GBM接受T244治疗后(部分病人已接受治疗2-3年)并无任何严重不良事件
• 预计2019年得到欧盟CE认证
• 在儿童脑瘤的应用有望获得FDA人道用途器材的免除(Humanitarian Device Exemption)
• T244日本权益已出售给一家知名药企
15、项目T239:基于 PARP抑制剂的诊断兼治疗平台
项目背景:近几年肿瘤领域的靶向疗法,若要说起最夺人眼球的,竞争最为激烈的,不得不提到PARP抑制剂。Leerink预测,PARP抑制剂在卵巢癌领域的销售峰值有望达到20亿美元。
迄今为止,获批的产品有3个,全球处于活跃状态的PARP抑制剂高达40多个。作为PARP抑制剂的同类第一产品,AstraZeneca的Olaparib在2014年批准用于卵巢癌的治疗后,临床试验在乳腺癌、胰腺癌、胃癌等领域广泛开展。
中国上市的PARP抑制剂只有Olaparib。除Olaparib之外,再鼎从Tesaro手中拿到的Niraparib以及百济神州的Pamiparib进展最快,目前均处于III期。T239是一款放射性标记的PARP抑制剂产品,除了治疗以外,还兼具检测等多功能。
公司介绍:这是一家位于德国的生物技术公司。其创始者及CEO是多轮创业者,曾成功的将两家生物技术公司完成出售,一家于2015年卖给Ipsen,一家2004年卖给Eckert & Ziegler AG。
产品优势:
• 竞争者进入壁垒高
• 多功能:诊断、生物标志物、治疗、影响观察
• 放射性核素半衰期短,局部能量高,辐射范围很短,以避免损害健康组织
• 暂无其他临床期的类似产品
• 已完成人体和动物的概念认证
16、项目T326: 具有超高增殖性、安全性,选择性、杀伤性的溶瘤病毒疗法
项目背景:自从2015年美国FDA批准安进公司的溶瘤病毒lmlygic (T-Vec) 治疗黑色素瘤后, 各大公司也纷纷涌入该领域。2018年2月,默克公司以3.94亿美元收购澳大利大生物技术公司Viralytics Limited, 同年5月,强生公司斥资10亿美元收购Benevir Biopharm, 增强其肿瘤免疫治疗的实力,2018年9月勃林格殷格翰又以2.44亿美金收购奥地利专注于的ViraTherapeutics。中国有包括北京阿克赛诺、成都康弘、成都法玛在内的五家公司进入临床期研究。2018年11月杭州阿诺医药出资866万美元从加拿大Oncolytics Biotech获得旗下溶瘤病毒产品 Perlareorep在大中华区、新加坡及韩国的独家开发和销售权利。尽管溶瘤病毒疗法在某些恶性肿瘤上取得了突破性进展,但仍存在着安全性、增殖有限、肿瘤之间的疗效差异等风险和问题。项目T326就是一款具有双重作用机制可以特异靶向治疗多种癌症和高效增殖的全新溶瘤病毒治疗平台。
公司介绍:一家专注于溶瘤病毒疗法的以色列生物技术公司,其技术平台是基于希伯来大学20年的科研成果。公司已完成对12名恶性多形性脑胶质瘤病人的I/II期安全和有效性评价,显示出了出色的安全和有效性。黑色素瘤、直肠癌和肺癌已进入临床前研究,并在动物模型上取得了显著地肿瘤杀伤效果。



平台及产品优势:
• 平台对于多种癌症具有极高的靶向性和选择性,并在人体内无清除抗体
• I/II期临床在大病毒注射计量下依然表现出超高的安全性
• 宿主实体瘤内的高效增殖能力,解决了溶瘤病毒疗法增殖有限的问题
• 双重作用机制:直接杀伤癌细胞及激发机体免疫反应
• 平台具有延展性可与多种疗法如化疗及免疫检查点结合
• 公司在达到第一个里程碑后会寻求在纳斯达克上市
17、项目T332:和多家国际药企合作的靶向G蛋白偶联受体的药物平台及首创新药
项目背景:G蛋白偶联受体(GPCRs)是人类最大的膜蛋白家族,能够调控广泛的生理过程。GPCRs一直是药物研发的重要靶点之一,靶向GPCRs的药物销量约占全球市场的27%,获得美国FDA批准的靶向GPCRs药物约有475个,占所有FDA批准药物总数的34%。GPCRs通常可以激活多条信号通路,偏向性的激发合适的信号通路增强药物的特异性降低毒性逐渐成为靶向GPCR药物研发的新思路。GPCR的别构调节剂(allosteric modulator)是一条药物研发的创新方向。别构调节剂可以远程的调控生理配体与受体结合引发的受体活性,与传统的GPCR靶向药物相比,具有更好的时间与功能上的特异性。项目T327具有完善的别构调节剂和偏向配体(biased ligand)的筛选平台还有多个潜在治疗肿瘤和中枢神经系统疾病的首创新药。
公司介绍:一家处于临床阶段专注于靶向G蛋白欧联受体药物筛选和研发的公司。公司采用全新的运营模式,囊括五家具有单一候选药物的附属公司。其中第一家治疗帕金森的附属公司已于2018年被某跨国制药公司以数亿美金收购。公司还与六家全球前20的大型制药公司签订了首创靶向GPCR新药的合作与授权协议。
产品和平台优势:
• 完善的别构调节剂与偏向受体筛选平台,已同三家全球前20制药公司签订合作协议,用于神经系统和肿瘤等多种疾病的药物开发
• 同类第一靶向PlexinA4 的激动剂
• 潜在的同类最佳的帕金森治疗药物
• 与全球前五的制药公司签订最终价值可高达2.7亿美金的抗肿瘤候选药物研发协议
• 另一款候选药物可重塑胰腺癌肿瘤微环境及血管正常化,可与多种疗法联合使用
18、项目T337: 同类第一无诱导耐药菌株的抗真菌药物
项目背景:近几年,随着免疫缺陷疾病患者增多、广谱抗菌药滥用、免疫抑制剂大量使用等因素的综合作用下,真菌感染发病率不断提高,每年因真菌感染死亡的人数高达150万人, 推动了抗真菌药物市场的快速增长。2017年中国抗真菌药总体市场突破240亿元,而全球市场总量更是高达118亿美金。虽然抗真菌药需求增长快,但如何降低真菌耐药性并且研发出高效低毒性的药物仍是企业面临的主要挑战。2019年6月恒瑞医药与美国Mycovia达成了最终可高达1亿美金的协议引进其治疗和预防多种真菌感染的先导化合物VT-1161。VT-1161对真菌的CYP51的选择性现有常用唑类抗真菌药,并且显示了较好的药代动力学特征、疗效和安全性。项目T337依托于其独有的天然产物化学平台研发出了安全耐受性好并无诱导抗药菌株的新型抗真菌药物。
公司介绍:一家处于临床期致力于抗真菌药物的制药公司。公司主要产品候选物已经入I期临床, 并与全球前五的制药公司签订了授权许可协议。
产品和平台优势:
• 新型靶点具有广谱性和有效性,无药物相互作用及无诱导耐药菌株
• 在动物实验中显示了较好的安全性和有效性
• 独有的天然产物化学平台可以快速合成上百种衍生物并适用于工业化生产
• 较强的专利保护
19、项目T286:一款7亿美元潜在年销售额的临床III期505(b)(2)苯达莫司汀寻求合作
项目背景:Non-Hodgkin’s Lymphoma (NHL, 非何杰金氏淋巴瘤) 和 Chronic Lymphocytic Leukemia (CLL, 慢性淋巴细胞白血病) 是两种常见的血癌,每年仅在美国的新增病例就分别有72,000和20,000个。虽然针对CLL目前有很多正在试验的治疗手段,比如化疗加干细胞移植,CAR-T细胞疗法等等,但是都距离批准和上市还有很长的一段时间,因此化疗依然是目前受到推荐的主流治疗手段。
Bendamustine (苯达莫司汀) 是一种在美国上市的注射用化疗药物,早在2008年就由Cephalon公司首先开发销售,业绩可观,并于2011年被Teva Pharmaceuticals收购。而Eagle Pharmaceuticals的Bendeka上市后同样被并被Teva收购,随后Bendeka逐渐成为美国主要的的苯达莫司汀产品。
T286主要活性成分为苯达莫司汀,用于血癌的治疗,辅药成分完全无毒,不给病人添加代谢负担,目前已经成功进入505(b)(2) NDA申报阶段,且FDA已经同意该项目不再需要其他临床测试数据。
公司介绍:该企业是一家加拿大公司,拥有由MBA, JD, MD 和PhD等专家组成的管理团队。团队不仅对癌症药物有丰富的研究,经验丰富的咨询师和法律专家更是对药物专利和FDA批准过程有深入的理解。
平台及产品优势:
• FDA孤儿药认证
• 已经进入最终505(b)(2) NDA申报阶段,无需额外临床试验
• 只有单一竞争者:Teva Pharmaceuticals 。苯达莫司汀2018年销售为6.42亿美元
• 相比竞争药物Bendeka具有多种优势:辅药成分无毒,不给病人添加新陈代谢负担,不需冷藏保存,在注射时用盐溶液稀释后依然可以在室温保持稳定活性24小时
• 成分专利2031年过期
• 还有另外一个基于赛诺菲Jevtana的505(b)(2)药物
20、项目T338: 《Global Health & Pharma》杂志评为代谢疾病疗法的领军企业
项目背景:以糖尿病、肥胖、非酒精脂肪肝为代表的代谢疾病已成为人类健康的重要威胁。2019年全球预计将有6亿肥胖和超过5亿的糖尿病人群。中国有超过1.14亿的糖尿病人群,居全球第一,肥胖人群也接近9000万人。此外,中国约有33%的人群患有非酒精脂肪肝。调节人体内的荷尔蒙分泌是治疗这些疾病的重要手段之一。以二型糖尿病为例,虽然以胰岛素注射为代表的疗法可以有效控制血糖水平,但这些疗法会引起胰岛素抗拒、胰岛素水肿、低血糖等诸多不良反应。项目T338研发的口服肠促胰岛素就为代谢疾病的治疗提供了一种全新的安全有效的方法。
公司介绍:一家处于临床前期致力于开发肠促胰岛素用于代谢疾病治疗的公司。公司采用全新的保健品/功能食品销售与药物研发的混合发展模式。2019年被欧洲《Global Health & Pharma》杂志评为代谢疾病疗法的领军创新企业,并且为全球前500的DEEP-TECH创业公司。
产品和平台优势:
• 保健品/功能食品的毛利率高达85%
• 细胞和动物实验显示了良好的安全性和耐受性,可明显促进GLP-1的释放
• 开发保健品/功能食品和药品,兼顾短期收益和长期发展
• 口服给药,提高病人的顺应性
• 中国糖尿病、肥胖、非酒精脂肪肝人群庞大,具有较大的市场空间及增长潜力
21、项目T290:全球唯一的口服式三氧化二砷抗癌药物
项目背景:目前Arsenic Trioxide (ATO, 三氧化二砷) 作为癌症治疗手段,已经在Acute Promyelocytic Leukemia (APL, 急性前髓细胞性白血病) 中使用,并在其他骨髓病变中也颇有发展前景。但现有的药物需要对病人进行长达144天的静脉注射,每天2至4小时,在实际医疗操作中非常不便,而且容易出现血管注射导致的感染,给病人和国家医疗体系带来了很大的负担。T290针对这一难题,研发了可口服的三氧化二砷胶囊,有望为三氧化二砷药物带来更大的市场。实际上,传统中药“雄黄”就是砷类药物,已经在中国的临床试验里取得了一些成果,但是由于雄黄是中药,不属于三氧化二砷,无法在美国和欧洲市场发展。
公司介绍:该企业总部设立于美国特拉华州,致力于发展口服式三氧化二砷,以改进现有的血癌治疗手段。其创始人之一曾是Incyte国际药企的创始人之一,曾经对JAK通路的药物发展和上市做出了巨大贡献,在癌症药物领域有非常丰富的经验。管理团队都曾在罗氏,诺华等国际药企担任要职。
平台及产品优势:
• 产品已经准备进入502(b)(2)临床III期试验
• 唯一的口服式三氧化二砷,比原有静脉注射方式更简单,更方便,更安全
• 药品颗粒较小,胶囊溶解快,化学成分稳定
• 已经具备大规模生产模式,领导团队拥有丰富的肿瘤学经验
• 有望与其他药物一同使用,用于其他骨髓类病变
22、项目T287:一个取代传统关节内注射的临床III期静脉注射关节炎药物
项目背景:骨关节炎是美国医院面对的造价最高的病情之一。发病率随着年龄而增长,但也受到基因、肥胖症、关节受伤等因素的影响。病人的疼痛和关节僵硬会逐渐加重,甚至会严重影响日常生活。目前骨关节炎并没有令人满意的治疗手段,病人主要通过辅助设备、止痛剂和关节内药物注射 来减缓病情,往往最终只能接受手术进行人工关节更换。项目T287针对这一问题,对两种已知安全的药物进行整合,研发出了一年只需静脉注射一次的药物,不仅可以减轻疼痛,并且可以修复骨髓损伤。
公司介绍:总部设立于美国宾夕法尼亚州,是BioNJ和Life Sciences Pennsylvania的成员组织之一。该公司专注于风湿病、免疫病和癌症的药物收购、发展和商业化。目前针对骨关节炎的项目T287是他们的主要产品。其CEO曾将5个产品推进上市。
平台及产品优势:
• 该产品两种已批准药物的新配方,即将进入临床III期试验
• 和已批药物相比,副作用更小 (13% VS 56%)
• 一年只需静脉注射一次(美国定价约$1,200/年)就可减轻病人疼痛,并且修复骨髓损伤
• 拥有3个美国专利,4个国际专利
• 骨关节炎目前缺乏有效药物和疗法,市场潜力大
• 预计2023年上市,第一年预期销售额为1-2亿美元
23、项目T288:一个肿瘤领域靶向纳米给药平台
项目背景:肿瘤坏死因子TNF-alpha通过结合肿瘤细胞表面受体,诱导细胞凋亡或坏死,对肿瘤以及肿瘤血管生长的抑制效果明显,但直接全身给药的系统毒性太大,使得TNF-alpha裸药的人体耐受剂量(200 ug/m2)低于药物有效浓度(500 ug/m2)。药物传递的高效性,特异性是新一代药物开发的关键考虑因素之一。
公司介绍:一家临床阶段专注肿瘤领域新型药物开发的公司,全球化的科研顾问团队。现有两个的候选药物。一款药物是纳米粒子单纯用于递送TNF-alpha, 已经完成了临床I期试验,美国国家癌症研究所同意免费为此公司开展针对胰腺癌的临床II期试验,该公司只需提供药物。
此临床试验预计在2022年。另一款药物则是在第一款药物的基础上增加了同时递送疏水性小分子抗癌药物紫杉醇或阿霉素的能力,正在准备申报IND。该纳米剂型的技术平台拥有多项专利。
产品优势:
• 在TNF-alpha临床期药物中唯一可以高剂量系统给药的候选药物
• 临床I期完成,无不良事件
• 此纳米药物剂型可极大提高给药剂量,同时降低全身毒副作用
• 此纳米药物剂型可被动靶向至肿瘤,进一步提高肿瘤部位的药物浓度 (是传统给药方式的646倍)
• 平台技术模块化,可以和化疗等联合使用,也可适用于TNF-alpha以外的分子,如IFN-gamma, Avastin, PD-1抗体等
• 在中国开启临床试验持开放态度
24、项目T350: 拥有29个专利保护的共晶平台提供多个505(b)(2)药物合作机会
项目背景:共晶工程可用于改善一种或多种物理性质,例如溶解速率及活性药物成分的稳定性。T331这家企业创建了一种专有的共结晶技术,该技术能结合L-茶氨酸,一种绿茶中发现的非蛋白质氨基酸,和已知获批药物共同创造出新的共晶体,一方面能显著改善产品性能,另一方面也能延长药品专利寿命,此外,还能有效的穿越血脑屏障。
公司介绍:通过此平台共晶技术,公司已成功重新配制了36种获准的原料药,涵盖各种药物类别(CNS、心脑血管、炎症、感染、HIV,癌症等),并将根据特定市场,比如中国市场的需求,重新配置新的药物。
其主要产品是茶氨酸和阿司匹林的新型共晶形式,可以增强溶解度,并阿司匹林有协同抗凝作用。正在开发的产品包括舌下服药以及静脉内注射。目前,因为阿司匹林溶解性差并会在血浆里快速水解,阿司匹林的静脉注射尚未被FDA获准使用。因此其静脉注射配方属于505(b)(2)审批通道。
产品和平台优势:
• 共晶平台提供505(b)(2)通道机会,降低成本及风险
• FDA及日本监管部门批准茶氨酸用于保健品,因此没有安全顾虑
• 茶氨酸和阿司匹林的新型共晶在人体试验中显示良好的安全性及药效,并有潜力克服阿司匹林的耐药性
• 拥有12个美国和17个海外专利,中国专利是2014年授权
25、项目T334: 延长药品专利保护及改善治疗效果的纳米给药平台
项目背景:近几年来,大型制药公司纷纷面临由于畅销药专利到期而引发的销售额和利润锐减的风险。辉瑞的明星降脂药物立普妥上市20年来累计销售额达1411亿美元,而在2011年专利到期后,其年销售额由2011年的95.7亿美金下降至2016年的17.5亿美元。据统计,由于专利到期全球制药行业将在2017-2022期间损失高达1940亿美金的销售额。随着新药研发成本的不断提高,如何延长和保护药物的专利和提高其原有的表现成为各大制药公司需要解决的问题。纳米药物通过将药物包裹在纳米材料内可以解决难溶性药物分子的输送问题、改善药物的代谢动力学性质提高药物的血液半衰期、并且能够降低药物的脱靶毒性。比如,新基(Celgene)的白蛋白结合紫杉醇纳米粒(Abraxane)可特异性的在肿瘤组织富集,提高了紫杉醇的血液半衰期,降低紫杉醇原有的心脏毒性,在2017年全球销售额达9.92亿美元。项目T334通过其全新的分子纳米包封技术达到改善药物表现增强专利保护和提高溢价的目的。
公司介绍:一家专专注于纳米给药系统的生物技术公司,共有四个产品处于临床或临床前阶段。公司的纳米包封技术更是在2017年获得了英国皇家化学学会评选的下一代技术大奖。公司与多家公司签订了对外许可和战略合作协议其中就有两家全球前40的制药公司和全球前十的农业公司。通过对外许可协议,公司最终可获得平均高达10亿美金的收入。
产品和平台优势:
• 纳米包封技术平台不仅用于给药困难的难溶性小分子药物,还可用于多肽、蛋白及核酸等大分子的给药,兼容性好
• 纳米包封技术平台可用于多种疾病的治疗,延展性好
• 目前在研的基于纳米技术的眼药水优于市场领导者,另一款用于过敏性结膜炎治疗的药物目前市场上无类竞争者,并且市场规模高达每年4亿欧元(约4.48亿美金)
• 公司从成立之初现金流一直为正
26、项目T305:一个II期微米级I/O新靶点免疫检查点抑制剂寻求合作
项目背景:肿瘤微环境中大量的免疫检查点受体被激活,导致了免疫抑制,且免疫检查点受体的表达水平和肿瘤进展的严重程度成正相关。肿瘤内注射免疫检查点受体抑制剂可以改变肿瘤免疫抑制微环境。巨噬细胞和树突状细胞等免疫细胞更倾向于吞噬纳米/微米直径的颗粒,利用这一特点可以将小分子药物更有效地靶向递送给免疫细胞。
公司介绍:该公司管理团队的成员均在各大国际制药巨头企业有过几十年的药物研发经历。公司CEO在生物制药领域有过成功创业,并购,融资 (> $400M), IPO等丰富经验,先后申报过4个NDA,包括Actonel的上市。现有一个临床前的肿瘤免疫疗法候选药物,是包裹免疫检查点受体阻断剂小分子的微米颗粒,通过肿瘤内注射的方式在动物体内中达到了30%的完全缓解率。计划在2020年末针对晚期头颈部鳞状细胞癌和肝癌提交IND (新药临床试验申请)。
产品优势:
• 新型靶点:阻断一个新型免疫检查点受体,和PD-(L)1和CTLA-4抑制剂联用有协调作用
• 微米粒子剂型具有靶向免疫细胞和长效缓释药物的优势
• 肿瘤内注射比类似的口服药物(临床二期)具有更好的免疫细胞靶向效果,更高的局部药物浓度,更高的生物利用度和更低的系统毒副作用
• 无类似药物竞争
• 研发和创业经验丰富的管理团队
27、项目T327:偏头痛100%响应的临床II期产品
项目背景:全球范围内,近15%的人遭受偏头痛的困扰,这给社会带来极大的经济负担。
目前常用的疗法包括镇痛药、曲坦类药物、β受体阻滞剂等,但这些疗法目前存在副作用大、疗效不足和患者依从性差等方面的问题,部分患者因副作用而被迫停止治疗。因此,开发新的偏头痛疗法需求强烈。
降钙素基因相关肽(CGRP)是偏头疼中产生痛觉的物质之一,基于此机理,多家生物药企积极开发靶向CGRP的单克隆抗体,包括安进的AMG334,Teva的TEV-48125,以及礼来的LY2951742。因为巨大的潜在市场,竞争非常激烈,也引发了不少专利的纠纷,此外,这种治疗方案只对50%的病人有效。T327同样也是针对某种和偏头痛相关的受体,从目前的数据来看,对100%的病人有效。
公司介绍:一家临床阶段的生物技术公司,专注开发针对偏头痛,帕金森病,阿尔茨海默病,肌萎缩侧索硬化症和其他中枢神经系统疾病的药物。项目T327属于药物重新利用(Drug repurposing), 之前已经在欧洲上市,治疗急性髓性白血病。
产品和平台优势:
• 60亿美元的市场
• FDA批准开始临床II期的开发
• 在墨西哥已有II临床数据,开发风险较低
• 从现有临床数据来看,T327(100%响应率)比CGRP抗体更强大
• 美国三项授权专利
28、项目T328: 一款新型CDK4 / 6/9口服抑制剂药物
项目背景:自从2015年全球首个CDK4/6抑制剂,辉瑞的哌柏西利获得美国FDA批准后,CDK4/6抑制剂就成为近年很热门的靶点。目前,美国FDA总共批准了三个CDK4/6抑制剂药物,其余两个是诺华的Kisqali以及礼来的Abemaciclib。2018年8月哌柏西利也成功在中国获批。2019的ASCO年会上诺华的Kisqali在III期晚期乳腺癌试验中提前到达终点,成为了唯一一种在晚期乳腺癌中表现出优异总体存活率的CDK4 / 6抑制剂。
国内药企也纷纷围绕已上市的药物进行结构改造,比较领先的包括恒瑞(III期)、四环、益方、东阳光、复星、贝达等等。
除了CDK4/6外,CDK9也是近期热门的靶点,开发此靶点的企业包括拜耳,阿斯利康等。项目T328是一款靶向CDK4/6/9的口服小分子药物,预计2020年完成IND申请。
公司介绍:一家私人控股的小型制药公司,致力于开发用于癌症和病毒性疾病多方面治疗的新型化合物,专注于新型,选择性,宿主细胞激酶靶向抑制剂。公司的目标是希望能在临床前阶段将产品的权益授出。
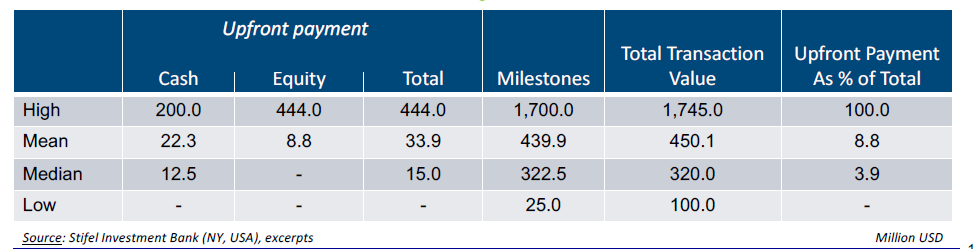


▲临床前阶段肿瘤药物授权历史数据
平台及产品优势:
• 同时靶向CDK4、CDK6和CDK9
• IC50为100nM,比现有的CDK4/6抑制剂 (IC50为10,000nM) 低
• 体外试验显示能和免疫疗法有很好的协同作用
• 专利2039年过期
• 有潜力克服CDK4/6抑制剂的耐药性
• 在多种动物肿瘤模型中显示良好的药效
• 动物模型实验中,未发现类似哌柏西利药物等停药后的反弹
29、项目T360: 全球第一家专注开发和商业化儿科肿瘤药物的公司
项目背景:2018年,FDA首次打破了自1996年以来批准新药的记录,其中超过一半的都是孤儿药。尽管如此,儿科癌症作为罕见病的一种,在过去40多年种,仅有四种药物得到获批。因为稀缺,EUSA Pharma的Erwinaze在获批后一年销售额就达到了1亿美元,在第二年将近2亿美元。而另外一个儿科肿瘤药物vincristine,辉瑞作为如今唯一供应商,供不应求,FDA出面表示会和辉瑞紧密合作,确保这种关键的抗癌药物可供需要的患者使用。
FDA为了激励企业开发罕见儿科新药,设立了优先审核凭证(PRV, Priority Review Voucher)。PRV可加快市场准入和创收。此外,PRV的持有人也可出售此项权利给第三方。迄今为止,已经批准的23种PRV中有15个被出售,累计销售价格为10亿美金。在2015年, United Therapeutics 便以3.5亿美元的价格向AbbVie出售了PRV。
公司介绍:专门致力于开发和商业化儿科肿瘤药物,成为儿科肿瘤药物的全球领导者。该公司一方面自主研发新的肿瘤药物,另一方面也积极获得临床阶段的资产许可,丰富管线。公司CEO有着丰富的管理背景,22岁就出售了自己的第一家公司。当他的儿子六岁时被诊断出患有髓母细胞瘤后,创建了儿童癌症基金会非盈利组织。
平台及产品优势:
• 全球第一家专注开发和商业化儿科肿瘤药物的公司。
• 和欧洲及美国最大的儿科临床机构达成合作,如ITCC和Children’s oncology group。
• 其主要候选药物是从Boehringer-Ingelheim获得,为一种高效的Polo样激酶1(PLK1)抑制剂,已完成在儿童临床I期试验,针对白血病和晚期实体瘤。
• 临床II期剂量已经确定,在成人的剂量之上。
• 临床 Ib/II期试验计划2019年在欧洲启动,针对儿童横纹肌肉瘤。
• 自主开发的成神经管细胞瘤药物已经进入临床前阶段
30、项目T285:一个与强生合作表观遗传领域第一的癌症药物筛选平台
项目背景:表观遗传自从1983年被发现和肿瘤发展有关后,已经有可观数量的靶向表观遗传的药物得以获批,包括Celgene的Vidaza、默克的Zolinza以及深圳微芯生物科技的Epidaza,这些药物大部分都是靶向DNMT或者HDAC,也在临床试验验证了这种药物开发思路的潜力,但缺乏精准性。此公司根据这一问题,设计了高通量筛选平台分析表观遗传特征来寻找使癌症细胞分化成良性细胞的同类第一、同类最优的药物,并配合使用生物标记物来实现精准治疗。
公司介绍:该公司成立于2017年5月,同年9月加入加州圣地亚哥的Johnson & Johnson Innovation – JLABS。目前与Janssen Pharmaceuticals是合作伙伴。公司CEO拥有17年在大药企和生物公司的领导经验,并在近期完成了一项和日本及亚太地区的交易。
产品优势:
• 强烈意向针对中国特殊市场设计项目,并愿意以股份换取战略合作,计划2年内和中国合作伙伴申请IND
• 同类第一高通量药物筛选平台,并配合深度机器学习,比传统技术更快(100倍速度),及成本更低
• 目前用于多种癌症领域,但也有更广泛的应用,比如Huntington等,同时也在探索药物再利用。
• 不仅仅局限在平台技术,而且会针对平台筛选出的药物与药企合作共同推进产品上市
• 拥有强大专利保护,有100%拥有权
31、项目T354:创新机理有效控制纤维化的505(b)2临床II期NASH药物
项目背景:非酒精性脂肪肝炎(NASH)被业内视为肿瘤免疫疗法后的又一个新蓝海。尽管目前还没有获批药物,但其市场规模到2025年预测可达到300~400亿美元。NASH新药开发面临了很多挑战,好消息是,全球首个NASH新药obeticholic acid (OCA)获批在即。
中国企业,包括正大天晴、歌礼、广生堂等都在积极进行自主研发,近年来也频频引进海外候选药物,比如拓臻生物与GENFIT公司签署独家产品授权和战略合作协议;歌礼通过其子公司与3-V Biosciences就TVB-2640达成战略合作与大中华区独家开发协议,康哲药业通过其全资附属公司与Can-Fite公司签订了许可、合作与经销协议。
大多数NASH的管线都是将代谢作为主要作用机制(如下图所示),比如Genfit的elafibranor。然而并非所有代谢性疾病患者都会发展为NASH,并且调节代谢不一定能改善纤维化。项目T254通过调节NKT免疫细胞的功能,以全新的机理直接控制炎症和纤维化。
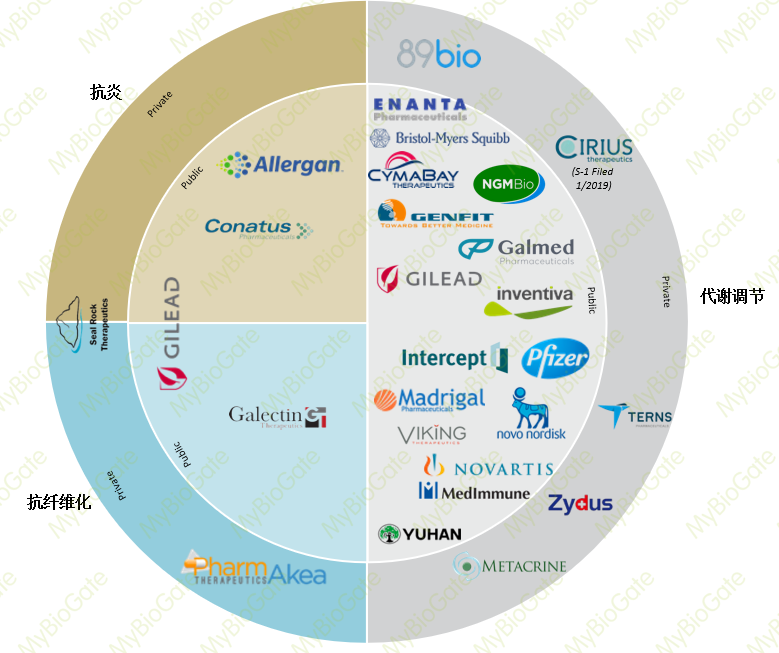


▲海外NASH竞争图谱(非穷尽)
公司介绍:一家处于临床阶段的生物技术公司,旨在从根本上改变炎症性疾病的治疗方式,重心为肝脏及自身免疫疾病。其CEO有超过20年的免疫疗法经验(肝脏,炎症,自身免疫,过敏和肿瘤科),在前一家公司担任CEO期间融资1亿美元,并成功上市。
平台及产品优势:
• 化合物专利保护到2023年
• 独特的作用机理,直接控制炎症和纤维化
• 准备临床II期阶段,此药物已获批用于另一适应症,505(b)2途径降低风险,并节省上市时间和成本
• 500+病人长达52周的观察中显示,T354可显著降低ALT
• 除NASH以外,针对特发性肺纤维化和急性酒精性肝炎的临床试验也正在筹备,此类疾病在中国的病发率呈上升趋势
32、项目T343: 华人CEO寻找下一代心脑血管重磅药中国合作伙伴
项目背景:心脑血管代谢病已逐渐成为人类健康的重要威胁,据统计,每年全球有超过1900万人死于心脑血管代谢疾病,医疗费用高达1.3兆亿美金,约占全球GDP的1.7%。根据《中国心脑血管病报告2018》概要显示中国心血管病人人数高达2.9亿,其中有2.45亿高血压。与此同时,中国有超过1.14亿的糖尿病人群及接近9000万的肥胖人群。基于最近20年超过1400篇文献及人体实验的研究发现,人体内产生的一种内源性多肽对上述疾病的调节与治疗起到了关键的作用。然而由于这种内源性多肽的体内半衰期只有不到8分钟,严重限制了它的治疗潜力。项目T343运用脂质体运载技术延长了内源性多肽的体内半衰期,提高了它对多种慢性病的治疗效果,有望成为潜在的下一代重磅药物。
公司介绍:一家致力于心脑血管代谢病治疗的临床前公司,公司的临床候选药物以完成研究性新药的申请工作。
产品及平台优势:
• 脂质体运载平台技术是斯坦福大学的研究成果,可用于不同多肽药物,延展性强,多肽药物市场价值高达250亿美金
• 脂质体运载平台可在1-2周内持续释放内源性多肽,并在动物心脏衰竭模型上显示了良好的安全性及有效性
• 脂质体运载的内源性多肽在二型糖尿病的动物模型上显示了逆转胰岛素抵抗的潜能
• 此脂质体技术还适用于其他小分子或者多肽药物,注射方式的话也可以实现多样化,除了静脉注射,也包括口服、吸入或者皮下注射等
• 中国心脑血管代谢病人群庞大, 具有极大的市场空间及增长潜力
• 很强的专利保护,专利是著名律所Morrison Foerster负责
33、项目T332:和多家国际药企合作的靶向G蛋白偶联受体的药物平台及首创新药
项目背景:G蛋白偶联受体(GPCRs)是人类最大的膜蛋白家族,能够调控广泛的生理过程。GPCRs一直是药物研发的重要靶点之一,靶向GPCRs的药物销量约占全球市场的27%,获得美国FDA批准的靶向GPCRs药物约有475个,占所有FDA批准药物总数的34%。GPCRs通常可以激活多条信号通路,偏向性的激发合适的信号通路增强药物的特异性降低毒性逐渐成为靶向GPCR药物研发的新思路。GPCR的别构调节剂(allosteric modulator)是一条药物研发的创新方向。别构调节剂可以远程的调控生理配体与受体结合引发的受体活性,与传统的GPCR靶向药物相比,具有更好的时间与功能上的特异性。项目T327具有完善的别构调节剂和偏向配体(biased ligand)的筛选平台还有多个潜在治疗肿瘤和中枢神经系统疾病的首创新药。
公司介绍:一家处于临床阶段专注于靶向G蛋白欧联受体药物筛选和研发的公司。公司采用全新的运营模式,囊括五家具有单一候选药物的附属公司。其中第一家治疗帕金森的附属公司已于2018年被某跨国制药公司以数亿美金收购。公司还与六家全球前20的大型制药公司签订了首创靶向GPCR新药的合作与授权协议。
产品和平台优势:
• 完善的别构调节剂与偏向受体筛选平台,已同三家全球前20制药公司签订合作协议,用于神经系统和肿瘤等多种疾病的药物开发
• 同类第一靶向PlexinA4 的激动剂
• 潜在的同类最佳的帕金森治疗药物
• 与全球前五的制药公司签订最终价值可高达2.7亿美金的抗肿瘤候选药物研发协议
• 另一款候选药物可重塑胰腺癌肿瘤微环境及血管正常化,可与多种疗法联合使用
战略需求:
寻求1600万美金的战略投资推动肿瘤微环境候选药物进入临床;寻求中枢神经和肿瘤候选药物的投资与合作。
34、项目T341:多个同类第一的口服双特异性小分子肿瘤免疫药物
项目背景:近几年,以检查点免疫抑制剂,如PD-1/PD-L1,为代表的肿瘤免疫治疗在基础和临床研究中取得了突飞猛进的发展。自2014年默克(Merck)的Keytruda和百时美施贵宝 (BMS)的Opdivo上市之后, 美国FDA共批准6款PD-1/PD-L1药物上市,用于超过14种癌症的治疗,其中Keytruda的2018年全年销售额高达71.71美金,而2019年预计将高达106亿美金。与此同时,以君实生物、恒瑞医药、信达生物、百济神州、基石药业在内的超过20家企业布局PD-1/PD-L1抗体,其中君实生物和信达生物的PD-1/PD-L1抗体于2018年底在国内获批上市。虽然据行业预测,中国PD-1/PD-L1的市场潜力高达460亿美元,但竞争日趋白热化,另一方面,抗体药物无法口服,且生产成本高昂,组织渗透能力有限。因此,如何寻找全新的安全有效的靶点且患者依从性高成为新一代肿瘤免疫治药物研发的关键。项目T341拥有针对多个全新肿瘤免疫治疗靶点的口服小分子药物。
公司简介:一家致力于肿瘤免疫疗法研发的临床前公司,其中三款候选药物将分别于2019第四季度、2020年第二季度及2021年第一季度进入一期临床研究。
产品及平台优势:
• 独有的技术平台可以快速筛选与靶向蛋白特异结合能力强的药物片段,已有200多个靶点的药物候选
• 口服小分子与抗体药物相比,提高了患者的依从性及组织渗透能力
• 用于治疗卵巢癌的双抑制剂在动物实验中显示了良好的安全及有效性,口服生物利用度大于20%,并显示了与紫杉醇、顺铂及PARP抑制剂的协同效应
• 用于治疗急性骨髓性白血病(AML)的口服双抑制剂在动物实验中显示了良好的安全,口服生物利用度高达50%以上。该药物的肿瘤生长抑制率高达100%,而同样用于治疗AML的Pacritinib(三期) 的肿瘤抑制率只有50%
• 全球范围内具有极强的专利保护
• 创新靶点(SIK; MELK;FLT3等),竞争者少
• 该公司将从某国际大药企购买一临床III期药物,进一步丰富其管线
35、项目T331: 被授予孤儿药资格认定的一氧化氮合成酶小分子抑制剂
项目背景:1998年,三名科学家因发现一氧化氮(nitric oxide , NO)作为心血管系统中的信号分子而获得诺贝尔奖。广泛的研究表明NO和心血管疾病、癌症、疼痛、阳痿等都有着密切的关系。NO有助于血管舒张, 从而影响动脉张力, 当过量产生的时候会导致低血压。T331通过抑制制造NO的一氧化氮合成酶(NOS), 从而防止NO诱导的血管舒张。
公司介绍:一家以色列临床阶段的生物技术公司,专门开发治疗和NO相关疾病的药物。
在临床2a临床试验中显示:接受T311注射的血液透析患者在透析大约2小时内能维持正常的血压变化,不需要额外的医疗干预。
产品和平台优势:
• T331作为血压稳定剂已经在东欧获批
• 有潜力针对多种适应症:低血压,偏头痛和头痛
• 强有力的知识产权保护(包括compositions of matter)
• 第一个针对透析低血压的孤儿药指定,获批后享有7年市场独占
•临床II期试验和世界最大的透析组织DaVita达成合作
神经领域
36、项目T342: 用于治疗抑郁和逆转癌症耐药性的同类最优的糖皮质激素拮抗剂
项目背景:糖皮质激素通过作用于糖皮质激素受体对人体中多种重要的生理活动进行调节。因此,糖皮质激素受体逐渐成为重要的治疗靶点。比如,糖品质激素拮抗剂米非司酮在库欣综合征、精神病性抑郁症、酒精使用障碍等疾病的临床研究中均取得了良好的效果。与此同时,过去十几年,越来越多的研究表明糖皮质激素受体在包括三阴性乳腺癌、非小细胞肺癌、卵巢癌、肾细胞癌在内的多种实体肿瘤过量表达,参与耐药性机制,并与患者的低生存率紧密相关。因此,阻断糖皮质激素受体为有效逆转癌症耐药性,提高病人生存率提供了新的治疗思路。2019年8月,位于美国湾区的ORIC Pharmaceuticals 完成了5500万美金 (约3.88亿人民币)的融资,使其总融资量超过1.75亿美金(约12.36亿人民币)推动其糖皮质激素拮抗剂候选药物ORIC-101进入二期临床用于多种实体瘤的联合药物治疗。
公司介绍:一家处于临床期致力于研发糖皮质激素拮抗剂的公司。其中,治疗精神病性抑郁症的候选药物已完成了临床二期研究。与此同时,同一候选药物用于癌症治疗的临床前研究也在同时进行。
产品和平台优势:
• T342从默克收购,且正在和两家国际药企谈合作
• 用于抑郁症的候选药物在13个临床一期、5个临床二期试验中显示了良好的安全性并可以明显提高促肾上腺皮质激素和清晨血清皮质醇的分泌含量
• 与米非司酮相比,候选药物显示了了对糖皮质激素受体更高的选择性和亲和力,并无堕胎效果,使其成为潜在的同类最优的糖皮质激素受体拮抗剂
• 候选药物能够在多种癌症细胞模型上逆转耐药性,显示了与化疗,放疗及免疫疗法联合使用的潜力
37、项目T291: 首个利用改变胃肠道微生物群治疗阿尔茨海默症的方案
项目背景:阿尔茨海默症是一种慢性的神经退行性疾病,其发病原因尚不明确,大部分的药物开发策略是通过靶向β-淀粉样蛋白斑或tau蛋白缠结来预防或治疗阿尔茨海默症,但至今还没有有效的治疗方法。在中国,大约 1000 万人被阿尔茨海默症困扰,居世界之首,且这个数字随着老年化将持续增长。
近些年来很多文献报道了关于胃肠道微生物群在脑疾病中的重要作用,包括阿尔茨海默症和帕金森等。一些科学家们提出:随着年龄的增长,人类胃肠道微生物群渐渐失去平衡,有可能逐渐引起炎症,加速淀粉状斑块的形成,最终导致神经元死亡。T291正是从这一角度入手,通过改变病人胃肠道微生物群(比如“粪菌移植”, Fecal microbiota transplantation, FMT),实现对阿尔茨海默症的预防和治疗。
公司介绍:该公司由多元化的专家团队成立,包括神经学教授和临床试验的管理人才。公司成立于2017年,总部设立在法国巴黎,临床研究中心等机构设立在欧洲其他国家。2018被选为瑞士值得投资的50家创业公司之一。
产品优势:
• 该公司有四种主要产品,分别为FMT、小分子药物、保健品和基因组测试。其中基因组测试已经进入临床I期试验
• 该药物产品为首个利用改变胃肠道微生物群针对阿尔茨海默症的治疗方案
• 一项研究报道了FMT针对自闭症儿童治疗的有效性及持久性(2年)
参考文献:Scientific Reports 9, Article number: 5821
• 强大专利保护,并且以后会根据新的菌株申请到更多专利
38、项目T176:根治癫痫的分子靶向药物发现平台
项目背景:癫痫是最为普遍的严重慢性神经系统疾病,全世界大约有五千万患者。由于脑神经细胞的异常活动,病人会反复经历癫痫发作,且发病频率随着年龄增长而增加。尽管在研药物(见下图),但它们只单纯控制癫痫发作的频率,治标不治本。T176利用专利保护的独特药物平台筛选出可以通过血脑屏障的创新型靶向药物,在小鼠和大鼠体内的药物实验取得了显著的成果。
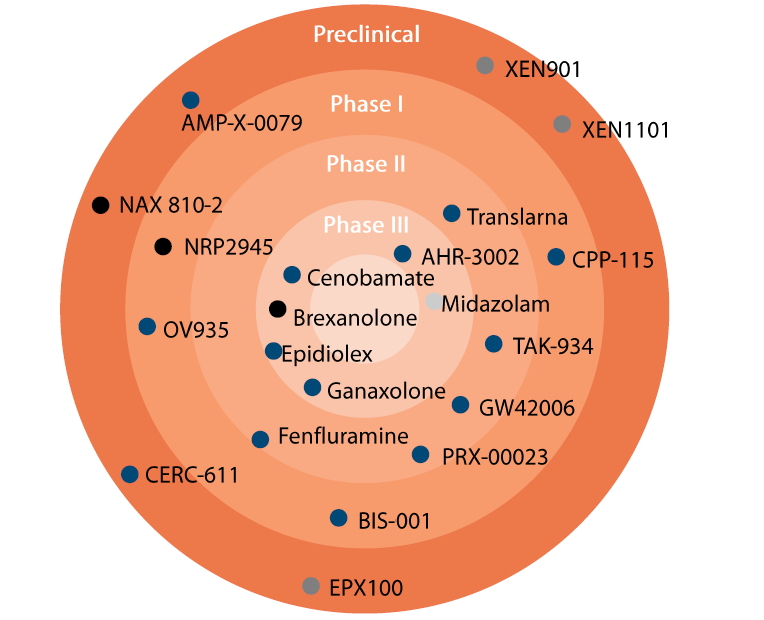


公司介绍:该公司坐落于西班牙巴塞罗那科学园 (Barcelona Science Park),从2011年成立至今已经对实验室进行了三次扩张。该公司与多所大学、研究中心和企业有战略合作关系,并且获得了美国国家卫生研究所(NIH)癫痫疗法筛选项目(ETSP, Epilepsy Therapy Screening Program)的支持。而且除了T176项目,该公司还在利用自己的药物平台同时对癌症和中枢神经系统疾病(精神分裂/帕金森等)进行药物研发。公司CEO被评为2019年十大欧洲年轻生物技术企业家。
产品优势:
• 拥有自己的药物筛选平台,且数据库里有超过一千万种未被研究的化合物
• 拥有分析蛋白结合度和细胞穿透力的技术,可以在实验室测试前进行计算机预测
• T176药物致力于对癫痫的疾病机理进行改良,从根本入手阻止疾病恶化;而其他正在进行测试的药物仅是控制癫痫发作频率
• 该公司除了T176,还在癌症和精神分裂症等其他疾病领域进行药物研发
公司CEO被评为2019年十大欧洲年轻生物技术企业家
39、项目T336:有望第一个上市的靶向beta淀粉样蛋白的阿尔茨海默症 (AD)药物
项目背景:阿尔茨海默式症 (AD)是一种多发于老年的神经退行性疾病,仅在美国就有570万患者,预计到2050年将增长到1400 万,医疗费用将高达1.1万亿。中国目前约有600万AD病人,并以每年30万的数量增长。目前美国FDA已批准的四种药物仅能缓解由AD引起的相关症状,并不能减缓疾病的进程。鉴于阿尔茨海默的巨大市场潜力,各大公司纷纷布局该领域,beta淀粉蛋白假说也为新药研发提供了可行的靶点。然而,靶向beta淀粉蛋白的药物研发却频频受阻。2019年7月安进与诺华宣布终止旗下beta淀粉样蛋白裂解酶(BACE)抑制剂的临床II/III期试验,而在2019 年3月百健(Biogen)和日本卫材(Eisai)就宣布终止其在三期的抗beta淀粉蛋白的单克隆抗体Aducanumab的临床研究。不仅如此,过去几年,礼来、默克、罗氏、阿斯利康、辉瑞等全球大型制药公司的候选药物也纷纷失败。最近几年的研究表明beta淀粉蛋白低聚物中间体才是导致神经元毒性的关键,而绝大多数失败的药物选择的靶点是早期的beta淀粉单体和晚期已经形成的斑块。项目T336就是研发能够靶向清除具有神经元毒性beta淀粉低聚物的阿尔茨海默药物公司。
公司介绍:一家处于临床期致力于治疗阿尔茨海默症在内的神经退行性疾病的生物制药公司。公司现有三个处于临床期与临床前的药物候选物。其中,AD候选药物将于2019年下半年进入临床三期研究,并获得美国FDA的快速申请审批资格。
产品和平台优势:
• 与其他失败药物相比,靶向具有关键作用的的beta淀粉低聚物
• 通过对1600名病人一年半的追踪,具有良好的耐受性和安全性,并无脑水肿
• 与抗体治疗药物相比,血脑屏障穿透率从0.3%提高到了40%
• 与静脉注射相比,口服治疗可以提高病人的依从性
• 与对照组相比,APOE4/4病人的认识和日常行为得到了显著性的改善
40、项目T222:人工智能诊断及药物开发平台,青光眼及阿尔兹海默症
项目背景:青光眼影响全球6000万人,是视网膜神经细胞死亡导致的视网膜结构的物理变化(萎缩)和不可逆的视力丧失。当前技术可以在视觉功能变化之前2年识别这些结构变化。T222技术使用标记有荧光染料的蛋白质来粘附应激和凋亡的细胞,并利用AI驱动的算法用于计算进行识别和分析,和现有技术相比,可提早8年识别此类结构变化,进而显著降低临床开发的风险。
公司介绍:这是一家英国生物技术公司,其技术是结合生物学、蛋白质和AI驱动的算法,能够在目前的护理标准之前检测青光眼、AMD,阿尔茨海默氏症,多发性硬化症和帕金森病。公司的CEO药学有着27年药企工作经验,曾在Allergan 、Nicox 、Visufarma 、Eli Lilly 、 Shire工作时推出过18种眼科产品。
产品优势:
• 可用于多种适应症
• 和现有技术比,可提早8年识别青光眼
• 已有9个机构有兴趣使用其产品协助临床开发(包括Genentech)
• FDA和MHRA被批准作为探索性药物开发生物标志物
• 作为诊断技术,已经处在临床III期
康复
41、项目增强膝盖康复能力
项目背景:国内目前针对康复领域的神经肌肉电刺激仪器市场非常混杂,例如增强锻炼肌肉等仪器。但是没有一项临床有效的康复仪器。
公司介绍:公司位于美国德州达拉斯。产品是一款可佩戴针对膝盖进行有效电刺激的器械。属于二类501K器械。能够帮助膝盖增强力量,加强活动能力,支持数据同步反馈。产品已经申请专利。
42、睡眠中促进康复能力
项目介绍:公司位于美国亚特兰大。具有多项产品针对手部,腿部,脚部,关节,肩膀和膝盖用于缓解疼痛,刺激循环,帮助康复。原理都是通过局部电刺激(可以是30分钟短时间或者8小时夜间疗程)。其中一款产品可佩戴式全掌感官电刺激手套,尤其可在睡眠时佩戴,来帮助中风病人恢复手腕手掌正常功能。用MRI扫描,发现在刺激后,部分小脑区血液循环发生改变。
女性健康
43、项目T325:用于提高女性健康和生活质量的革命性节育手段
项目背景:宫内节育器(IUD)是目前最有效和最流行的女性节育手段,有效率高达99%。全球目前约有2亿女性使用,市场销售额预计会在2024年突破54亿美金。中国有超过1亿女性使用宫内节育器,约占全球总使用人数的70%。尽管如此,宫内节育器目前仍面临很多问题。每年有超过5万例的穿孔, 超过10%的节育器会发生本体脱落,超过7%的节育器会发生错位。全球还有14%-25%的育龄女性伴有子宫异常出血。与其他治疗选择相比,子宫内膜去除术由于创伤最小且成功切除可避免长期用药等特点被逐渐广泛应用。但目前子宫内膜去除术需要住院治疗且价格昂贵,仅在美国每年就要花费超过120亿美金。因此,如何解决以上问题,成为了设计新一代提高女性健康及生活质量的宫内技术的重要指标。
公司介绍:一家处于商业和临床期的致力于女性健康的医疗器械公司。公司的独创宫内节育器已经上市,每年创造利润超过400万美金,全球约有8万女性使用。另一款用于子宫内膜去除术的产品已经入临床阶段,显示出了良好的安全性和耐受性。与同类产品相比,其手术花费可降低50%,便于使用,且无需额外的辅助仪器和人员培训,预计2028年收入会超过4亿美金。
产品优势:
• 与传统宫内节育器相比,降低疼痛和不规则出血,彻底消除节育器错位问题
• 与传统节育器相比,节育器穿孔率仅为0.05%,本体脱落低至5%
• 中国仍有超过半数育龄女性未使用节育器作为避孕手段,市场空间巨大
• 子宫内膜去除产品具有高性价比和便于使用等革命性特点,有利于市场渗透和定价
44、项目T101:防治宫内粘连
项目背景:中国女性现在普遍希望晚婚晚育,然而,随着年龄的增长,怀孕的可能也因很多因素而下降,其中,宫腔粘连(IUA)是导致不孕的一个最重要的原因。
宫腔粘连是由于妊娠或非妊娠子宫的创伤,导致子宫内膜基底层受损,使宫腔部分或全部闭塞从而导致月经异常、不孕或反复流产等。其本质是内膜纤维化。
宫腔镜是目前治疗宫腔粘连的有效手段。但是,这是一种创伤性手术,宫腔镜术中并发症可出现穿孔、出血、休克甚至死亡。
公司介绍:该公司位于法国蒙皮利埃。公司核心产品是一款可降解的宫颈防粘膜。产品有效成分是一种聚合物,放入子宫后30分钟后充实子宫,形成一个物理屏障防治子宫粘连,8天后之后自动降解,排出体外。产品在大鼠上已完成安全性和有效性实验。
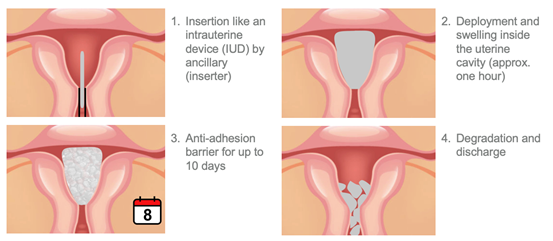


产品属于Class III器械,需要临床试验。预计在欧洲和中国完成试验审批。



识别二维码,填写“一对一”对接意向项目表
活动咨询
张晓嘉



WeChat:BioToChina


评论